欲使0.1 mol·L-1的NaHCO3溶液中c(H+)、c( )、c(
)、c( )都减小,其方法是( )
)都减小,其方法是( )
| A.通入二氧化碳气体 | B.加入氢氧化钠固体 |
| C.加水稀释 | D.加入饱和石灰水溶液 |
下列说法不正确的是
| A.磷酸的摩尔质量与6.02×l023个磷酸分子的质量在数值上相等 |
| B.6.02×l023个氮分子和6.02×1023个氢分子的质量比等于14:1 |
| C.32g氧气所含的原子数目为2×6.02×1023个 |
| D.常温常压下,0.5×6.02×1023个一氧化碳分子所占体积是11.2L |
下列有关海水综合利用的说法正确的是
| A.利用电解的方法可以从海水中获取淡水 |
| B.海水蒸发制海盐的过程只发生了化学变化 |
| C.从海水中可以得到NaCl,电解熔融NaCl可制备Cl2 |
| D.海水中含有钾元素,只需经过物理变化可以得到钾单质 |
铜粉加入稀盐酸中,加热无现象,这时加入一种盐则铜粉溶解而溶液变蓝,同时有气体放出,这种盐是
| A.NaCI | B.KNO3 | C.FeCl2 | D.Fe2(SO4)3 |
在恒温恒容容器中进行反应A(g) 2B(g)+C(g),若A的浓度由0.1 mol·L
2B(g)+C(g),若A的浓度由0.1 mol·L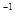 降到0.06 mol·L
降到0.06 mol·L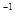 需20 s,那么由0.06 mol·L
需20 s,那么由0.06 mol·L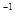 降到0.024 mol·L
降到0.024 mol·L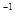 需要的时间
需要的时间
A.等于18s B,等于12s C,小于18s D.大于18s
若aXm+与bYn-的核外电子排布相同,下列关系式正确的是
| A.b=a-n+m | B.b-n=a-m |
| C.离子半径Xm+<Yn- | D.原子半径X<Y |