侯氏制碱法的步骤如下图所示: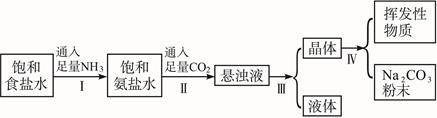
试完成下列问题:
(1)若上述的悬浊液是NaHCO3和NH4Cl的混合物,则I和Ⅱ的总反应式是________________。
(2)由这一反应可知NaCl比NaHCO3溶解度________________。
(3)操作I、Ⅱ不能颠倒的原因是 ________________。
(4)Ⅲ的操作叫 ________________;Ⅳ的操作叫 ________________________。
某化学实验室产生的废液中含有Fe3+、Cu2+、Ba2+、Cl-四种离子,现设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯化铁晶体。
(1)沉淀1中含有的金属单质是。
(2)氧化时加入H2O2溶液发生反应的离子方程式为。
(3)下列物质中,可以作为试剂X的是(填字母)。
| A.BaCl2 | B.BaCO3 | C.NaOH | D.Ba(OH)2 |
(4)制备氯化铁晶体过程中需保持盐酸过量,其目的是。
(5)由过滤2得到的滤液制备BaCl2的实验操作依次为、冷却结晶、、洗涤、干燥。
二氧化氯(ClO2)作为一种高效强氧化剂已被联合国世界卫生组织(WHO)列为AI级安全消毒剂。常温下二氧化氯为黄绿色或橘黄色气体,性质非常不稳定,温度过高或水溶液中ClO2的质量分数高于30%等均有可能引起爆炸,易与碱液反应生成盐和水。
(1)某研究小组设计如图所示实验制备ClO2溶液,其反应的化学方程式为
2KClO3+H2C2O4+2H2SO4 2KHSO4+2ClO2↑+2CO2↑+2H2O
2KHSO4+2ClO2↑+2CO2↑+2H2O
①在反应开始之前将烧杯中的水加热到80℃,然后停止加热,并使其温度保持在60~80℃之间。控制温度的目的是_____________。
②装置A用于溶解产生的二氧化氯气体,其中最好盛放_______(填字母)。
a.20mL 60℃的温水b.100mL冰水
c.100mL饱和食盐水d.100mL沸水
③在烧瓶中加入12.25g KClO3和9g草酸(H2C2O4),然后再加入足量的稀硫酸,水浴加热,反应后生成ClO2的质量为______________________ClO2
(2)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子(ClO2-)。饮用水中ClO2、ClO2-的含量可用连续碘量法进行测定,实验步骤如下:
步骤1:准确量取一定体积的水样加入锥形瓶中;
步骤2:调节水样的pH至7.0~8.0;
步骤3:加入足量的KI晶体;
步骤4:加入少量指示剂,用一定浓度的Na2S2O3溶液滴定至终点;
步骤5:再调节溶液的pH≤2.0;
步骤6:继续用相同浓度的Na2S2O3溶液滴定至终点。
①步骤1中若要量取20.00mL水样,则应选用的仪器是____________________________。
②步骤1~4的目的是测定水样中ClO2的含量,其反应的化学方程式为: 2ClO2+2KI=2KClO2+I22Na2S2O3+I2=Na2S4O6+2NaI,则步骤4中加入的指示剂为_________,滴定达到终点时溶液的颜色变化为___________________________。
③步骤5的目的是用I-将溶液中的ClO2-还原为Cl-以测定其含量,该反应的离子方程式为________________。
(14分) 芳香族羧酸通常用芳香烃的氧化来制备。芳香烃的苯环比较稳定,难于氧化,而环上的支链不论长短,在强烈氧化时,最终都氧化成羧基。某同学用甲苯的氧化反应制备苯甲酸。
反应原理:
反应试剂、产物的物理常数:
| 名称 |
相对分 子质量 |
性状 |
熔点 |
沸点 |
密度 |
溶解度 |
||
| 水 |
乙醇 |
乙醚 |
||||||
| 甲苯 |
92 |
无色液体易燃易挥发 |
-95 |
110.6 |
0.8669 |
不溶 |
易溶 |
易溶 |
| 苯甲酸 |
122 |
白色片状或针状晶体 |
122.4 |
248 |
1.2659 |
微溶 |
易溶 |
易溶 |
主要实验装置和流程如下:
实验方法:一定量的甲苯和KMnO4溶液置于图1装置中,在90℃时, 反应一段时间,再停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。
(1)无色液体A的结构简式为。操作Ⅱ为。
(2)如果滤液呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,加亚硫酸氢钾的目的是。
(3)下列关于仪器的组装或者使用正确的是。
A.抽滤可以加快过滤速度,得到较干燥的沉淀
B.安装电动搅拌器时,搅拌器下端不能与三颈烧瓶底、温度计等接触
C.图1回流搅拌装置应采用直接加热的方法
D.冷凝管中水的流向是下进上出
(4)除去残留在苯甲酸中的甲苯应先加入,分液,水层再加入,然后抽滤,干燥即可得到苯甲酸。
(5)纯度测定:称取1.220g产品,配成100mL溶液,取其中25.00mL溶液,进行滴定 ,消耗KOH物质的量为2.4×10-3mol。产品中苯甲酸质量分数为。
碳酸钙、盐酸是中学化学实验中的常用试剂。
(1)甲同学拟测定CaCO3固体与过量0.1 mol·L-1HCl的反应速率。
① 该反应的化学方程式为_________。
② 设计两种实验方案:
方案一:通过测量_________和__________计算反应速率
方案二:通过测量_________和__________计算反应速率
③ 配制250mL 0.1 mol·L-1HCl:量取___________mL 10 mol·L-1HCl加入烧杯中,加适量蒸馏水,搅拌,将溶液转入__________中,洗涤,定容,摇匀。
(2)乙同学拟用如图装置探究固体表面积和反应物浓度对化学反应速率的影响。
限选试剂与用品:0.1 mol·L-1HCl、颗粒状CaCO3、粉末状CaCO3、蒸馏水、量筒、秒表
① 设计实验方案:在固体表面积或反应物浓度不同的条件下,测定________(要求所测得的数据能直接体现反应速率大小)。
② 拟定实验表格,完整体现实验方案。(表格列数自定;列出所用试剂的用量、待测物理量和拟定的数据;数据可用字母a、b、c等表示)
| 物理量 实验序号 |
V(0.1mol/L HCl)/mL |
…… |
实验目的:实验1和2探究固体表面积对反应速率的影响;实验1和3探究反应物浓度对反应速率的影响 |
|
| 实验1 |
…… |
|||
| 实验2 |
…… |
|||
| 实验3 |
…… |
乙醛在催化剂存在的条件下,可以被空气氧化成乙酸。依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体)。已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全。有关物质的沸点见下表:
| 物质 |
乙醛 |
乙酸 |
甘油 |
乙二醇 |
水 |
| 沸点 |
20.8℃ |
117.9℃ |
290℃ |
197.2℃ |
100℃ |
请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为(注明反应条件)________________;
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置。在实验开始时温度计水银球的位置应在___________,目的是_____________________________;当试管A内的主要反应完成后,应进行蒸馏操作,温度计水银球的位置应在___________________。
(3)烧杯B内盛装的液体可以是____________(写出一种即可)。
(4)若想检验试管C中是否含有产物乙酸,在下列所提供的药品或用品中,可以使用的是____________。(填字母)
a.pH试纸b.碳酸氢钠粉末
c.红色石蕊试纸d.银氨溶液