有一包粉末状的混合物,可能含有MgCl2、FeCl3、NaOH、CuSO4、Al2(SO4)3、KNO3、CaCO3、NaCl中的两种或多种。将混合物置于水中搅拌,得无色透明溶液;再将所得无色透明溶液分为两份:一份中通入CO2,有白色沉淀出现,滴入稀盐酸沉淀消失;另一份中加入BaCl2溶液,同样有白色沉淀出现,此沉淀不溶于稀硝酸。完成下列问题:
(1)原混合物中肯定含有的物质是________(写化学式)。
(2)混合物置于水中,所得无色透明溶液中一定含有的物质是________(写化学式)。
(3)常温下所得无色透明溶液的pH________7(填“>”或“<”)。
(4)在所得无色透明溶液中有关离子方程为________________________。
X、Y、Z、W四种常见元素,其相关信息如下表:
| 元素 |
相关信息 |
| X |
空气含量最多的元素 |
| Y |
3p能级只有一个电子 |
| Z |
单质用于制造集成电路和太阳能板的主要原料 |
| W |
常见化合价有+2、+3,其中一种氧化物为红褐色 |
(1)W位于周期表的第周期,第族。
(2)用“>”或“<”填空。
| 离子半径 |
电负性 |
第一电离能 |
单质熔点 |
| X Y Z |
ZW |
XZ |
XW |
(3)X2、碳和Z的氧化物在1300℃时可合成Z3X4。写出该反应化学方程式。Z3X4是一种耐高温的结构陶瓷材料,是化合物(填“共价”或“离子”)。
(4)查阅资料知道:
4Y(s)+3O2(g)=2Y2O3(s) △H=-3351.4 kJ.mol-1
3W(s)+2O2(g)=W3O4(s) △H=-1120 kJ.mol-1
则Y与W3O4反应的热化学方程式是:。
某无色溶液X,由Na+、Ag+、Ba2+、Al3+、[Al(OH)4]--、MnO4—、CO32--、SO42—中的若干种离子组合,取溶液进行如下连续试验:(填化学用语)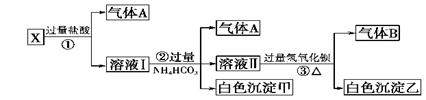
(1)气体A的成分是:_________________,气体B的成分是_____________
(2)X溶液中一定存在的离子是:____________________________
(3)写出步骤①发生反应的所有离子反应方程式:_________________________
(4)写出步骤②形成白色沉淀甲的离子方程式:______________________
(5)写出白色沉淀乙的可能组成:____________________________
炼金废水中含有络离子[Au(CN)2]+,其电离出的CN—有毒,CN-与H+结合生成HCN时,其毒性更强。回答下列问题:
(1)HCN的电离方程式为______________________NaCN溶液的pH_____7(填“< > =”)
(2)与弱电解质的电离方程式相似,[Au(CN)2]+也存在着两步电离,其一级电离方程式为________。
(3)处理这种废水是在碱性条件下,NaClO将CN—氧化为碳酸根和氮气,其离子方程式为:_______。
(4)在酸性条件下,ClO—也能氧化CN--,但实际处理废水时却不在酸性条件下进行的原因是_________。
(14)A、B、C、D、E、F是常见单质,其中A是用量最大,应用最广泛的金属;元素D是地壳中含量最多的金属元素;D元素和E元素在周期表中相邻。G、H、I、J、K、L是常见化合物,其中G在常温下是无色液体,H是黑色固体。以上物质相互间的转化关系如图所示:请回答下列问题: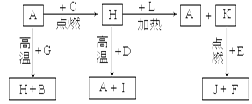
(1)元素A在元素周期表中的位置为周期族。
(2)写出K的电子式。
(3)写出H和D反应的化学方程式。
(4)D能与氢氧化钠溶液反应,请写出该反应的离子方程式。
(5)写出A与G反应的化学方程式。
(6)K与E反应时产生的现象有;该反应的化学方程式为 ______________。
(7)已知F的燃烧热为akJ/mol,L的燃烧热为bkJ/mol,试写出F生成L的热化学方程式__________。
(11)某校化学兴趣小组的同学对硝酸盐的受热分解进行探究。他们设计了如下装置分别加热了Ca(NO3)2、Cu(NO3)2、AgNO3三种固体。(加热及夹持装置未画出)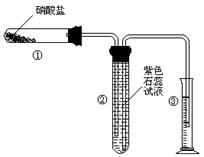
(1)甲同学加热的是Ca(NO3)2。加热过程发现:装置②中产生气泡,部分石蕊试液被压至装置③中;用带火星的木条检验②中的气体,木条复燃;分析装置①中剩余的固体得知,剩余固体中含有N元素,且显+3价。请写出Ca(NO3)2受热分解后生成产物的化学式:、。
(2)乙同学加热的是Cu(NO3)2。加热过程发现:装置②中也有气泡产生,但在上升的过程中消失。石蕊试液逐渐变为红色,液体几乎不被压至装置③中。装置①中的固体逐渐变为黑色。请写出Cu(NO3)2受热分解的化学方程式:;
(3)丙同学加热的是AgNO3。加热过程发现:装置②中也有气泡产生,但在上升的过程中气泡部分消失,剩余的气体也能使带火星的木条复燃。石蕊试液也逐渐变为红色,有少量液体被压至装置③中。装置①中的固体逐渐变为黑色。丙同学据此写出了AgNO3受热分解可能的两种化学方程式:
(Ⅰ)4AgNO3  2Ag2O+4NO2↑+O2↑,(Ⅱ)2AgNO3
2Ag2O+4NO2↑+O2↑,(Ⅱ)2AgNO3  2Ag+2NO2↑+O2↑。
2Ag+2NO2↑+O2↑。
Ⅰ、Ⅱ中正确的是,并说明理由:。
请你设计一个简单的实验证明你的结论是正确的:。
(4)由上述3个实验的结果,请你推测硝酸盐受热分解的规律:。
(5)标况下如丙同学操作,称量ag硝酸银,受热完全分解后,读取量筒体积为bml,求硝酸银的分解率:____________(化简成整数比例关系,可不用化成小数)