(本小题15分)A、B、C、D四元素的核电荷数依次增加,它们的离子的电子层数相同且最外层电子数均为8。A原子的L层电子数与K、M层电子数之和相等,D原子的K、L层电子数之和等于电子总数的一半。回答以下问题:
(1)四元素的符号依次是A______;B______;C________;D______。
(2)写出B、D元素的离子结构示意图:
B.______________________; D.______________________。
(3)用电子式表示A、C元素形成的离子化合物的过程:
________________________________________________________。
(4)在A、B、C、D最高价氧化物水化物中:
比较其中酸的酸性强弱:____________________________;
比较其中碱的碱性强弱:____________________________。
用VSEPR 理论判断:
| 物质 |
孤对电子对数 |
轨道杂化形式 |
分子或离子的形状 |
| NH4+ |
|||
| NCl3 |
按照下列元素基态原子的电子排布特征判断元素,并回答问题:
A原子中只有一个电子层且只含有一个电子;B原子的3p轨道上得到一个电子后不能再容纳外来电子;C原子的2p轨道上有一个电子的自旋方向与2p轨道上其他电子的自旋方向相反;D原子的第三电子层上有8个电子,第四层上只有1个电子;E原子的价电子排布式为3s23p6
(1)以下分别是哪种元素(用元素符号填空):
A:_____________; C:_____________;D:____________;
(2)B原子的核外电子排布式。
(3)E的原子结构示意图。
某温度下,在2L密闭容器中,3种气态物质 X、Y、Z的物质的量随时间变化曲线如图,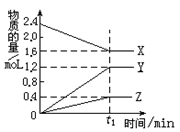
⑴① 该反应的化学方程式是_____________________。
②在t1min时,该反应达到了__________状态,下列可作为判断反应已达到该状态的是__________
| A.X、Y、Z的反应速率相等 | B.X、Y的反应速率比为2:3 |
| C.容器内气体压强保持不变 | D.生成1molZ的同时生成2molX |
⑵ ①若上述反应中X、Y、Z分别为NH3、H2、N2,且已知1mol氨气分解成氮气和氢气要吸收46kJ的热量,则该反应的热化学反应方程式为:__________________________。
②两位同学讨论放热反应和吸热反应。甲说加热后才能发生的化学反应是吸热反应,乙说反应中要持续加热才能进行的反应是吸热反应。你认为他们说法正确的是______同学。
A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,B与C的单质在加热条件下反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上的电子数之和。
(1)写元素符号:A为 ,B为 ,C为 。
D的最高价氧化物的水化物化学式是。
(2)写出A、B形成的化合物与E反应的化学方程式: 。
(3)E属(“离子”或“共价”)化合物。E中含键。
(4)D元素在周期表中位于第_____周期______族。
已知A、B、C、D为气体(其中A为黄绿色),E是常见的氮肥,F为固体,G是氯化钙,它们之间的转换关系如下图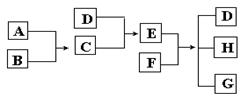
⑴ D的结构式是_____________,E的化学式(分子式)是_____________。
⑵ D和O2反应的化学方程式是______________________________。
⑶ E和F反应生成D、H和G的化学方程式是___________________________________。