A、B、C、D、E为中学常见的五种物质,均含元素Y,有的还可能含有元素X、Z,元素X、Y、Z的原子序数依次递增。
①元素Y在A、B、C、D、E中所呈现的化合价依次递增,其中只有B为单质;
②常温下将气体D通入水中发生反应,生成C和E;
③工业上以A、空气和水为原料,通过催化氧化法制取E。
请完成以下问题:
(1)B的电子式为___________,A的结构式为___________,A分子的空间构型是__________;
(2)写出②中涉及反应的化学方程式____________________________________;
(3)由B反应生成1 mol A放出的热量为46.2 kJ,写出该反应的热化学方程式,并注明反应条件________________________;
(4)工业上,若输送Cl2的管道漏气,用A进行检验时可观察到大量白烟,同时有B生成,写出有关反应的化学方程式________________________。
某有机物X的蒸气完全燃烧时需要3倍于其体积的氧气,产生2倍于其体积的CO2和3倍于其体积的水蒸气,有机物X在适宜条件下能进行如下一系列转化:
①有机物X的蒸气在Cu或Ag的催化下能被O2氧化成Y。
②X能脱水生成烯烃Z,Z能和HCl反应生成有机物S。
③S和NaOH水溶液共热生成溶于水的有机物X。
试完成下列问题:
(1)写出X的结构简式:________________________。
(2)用化学方程式表示①—③的转化过程。
请完成有关以通式CnH2n+1OH所表示的一元醇的下列问题:
(1)当n=0时,CnH2n+1就等于H。因此,有人说H—OH(水)是符合这个通式的,所以水是醇类的同系物。对吗?为什么?_________________________________________________
_______________________________________________________________________________。
(2)若有同类同分异构体时,n的最小值为_____________;不能发生分子内消去反应时,n(n=1除外)的最小值为_____________。
A是一种含碳、氢、氧三种元素的有机化合物。已知:A中碳的质量分数为44.1%,氢的质量分数为8.82%;A只含一种官能团,且每个碳原子上最多只连一个官能团;A能与乙酸发生酯化反应,但不能在两个相邻碳原子上发生消去反应。请完成下列问题:
(1)A的分子式是__________________,其结构简式____________________________。
(2)写出A与乙酸反应的化学方程式:______________________________________________。
(3)写出所有满足下列3个条件的A的同分异构体的结构简式。①属直链化合物;②与A具有相同的官能团;③每个碳原子上最多只连一个官能团。这些同分异构体的结构简式是____________________________________。
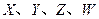 是周期表中原子序数依次增大的前20号元素。
是周期表中原子序数依次增大的前20号元素。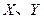 同周期。
同周期。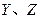 同主族,
同主族,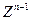 与
与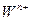 离子的电子层结构相同。由这四种元素形成的单质、化合物有如下图转化关系。已知:常温下
离子的电子层结构相同。由这四种元素形成的单质、化合物有如下图转化关系。已知:常温下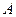 为液体,
为液体,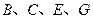 为气态化合物,且
为气态化合物,且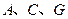 均为直线型分子;
均为直线型分子;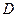 是由元素
是由元素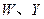 形成的常见化合物。
形成的常见化合物。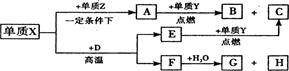
(1)元素W的名称,Z的原子结构示意图,A的电子式。
(2)写出D、E的化学式:D、E。
(3)①已知38gA与Y完全反应生成B、C时放出口aKJ的热量,写出该反应的热化学
方程式:
②F与水反应的化学方程式:
作为重要的工业三酸之一,硝酸通常有以下两种制取方法:
I.硝酸盐与浓硫酸反应: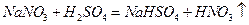
II.氨的催化氧化法,其主要步骤为:①氨的催化氧化;②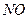 氧化成
氧化成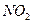 ;③水吸收
;③水吸收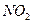
生成硝酸。
(1)方法l中不能加强热,其原因是。(2)写出方法Ⅱ中步骤①的化学反应方程式。(3)采用方法Ⅱ制取硝酸,若经过多次循环后,步骤②、③中氮元素的总利用率是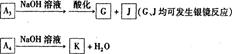
90%,某化工厂用1 t氨气制得5t63%的硝酸溶液,求步骤①中氨气的转化率?(书写计算过程,结果精确到0.1%)