可用于判断碳酸氢钠粉末中混有碳酸钠的实验方法是( )
| A.加热时有无色气体放出 |
| B.滴加盐酸时有气泡放出 |
| C.溶于水后滴加澄清石灰水,有白色沉淀生成 |
| D.溶于水后滴加BaCl2稀溶液,有白色沉淀生成 |
已知电极上每通过96 500 C的电量就会有1 mol电子发生转移。精确测量金属离子在惰性电极上以镀层形式沉积的金属质量,可以确定电解过程中通过电解池的电量。实际测量中,常用银电量计,如图所示。下列说法不正确的是( )
| A.电量计中的银棒应与电源的正极相连,铂坩埚上发生的电极反应是:Ag++e-=Ag |
| B.称量电解前后铂坩埚的质量变化,得金属银的沉积量为108.0mg,则电解过程中通过电解池的电量为96.5C |
| C.实验中,为了避免银溶解过程中可能产生的金属颗粒掉进铂坩埚而导致测量误差,常在银电极附近增加一个收集网袋。若没有收集网袋,测量结果会偏高。 |
| D.若要测定电解饱和食盐水时通过的电量,可将该银电量计中的银棒与待测电解池的阳极相连,铂坩埚与电源的负极相连。 |
化学方程式可简明地体现元素及其化合物的性质。已知氧化还原反应:
2FeCl3 + 2HI = 2FeCl2 + I2 + 2HCl; 2Co(OH)3 + 6HCl = 2CoCl2 + Cl2↑ + 6H2O
2Fe(OH)2 + I2 + 2KOH= 2Fe(OH)3 + 2KI; 3I2 + 6KOH=" 5KI" + KIO3 + 3H2O
复分解反应:2HSCN + K2CO3 =" 2KSCN" + CO2 ↑ + H2O; KCN + CO2 + H2O =" HCN" + KHCO3
热分解反应:4NaClO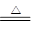 3NaCl + NaClO4;NaClO4
3NaCl + NaClO4;NaClO4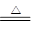 NaCl + 2O2↑
NaCl + 2O2↑
下列说法不正确是( )
| A.氧化性(酸性溶液):FeCl3 > Co(OH)3> I2 |
| B.还原性(碱性溶液):Fe(OH)2 > I2 > KIO3 |
| C.热稳定性:NaCl > NaClO4 > NaClO |
| D.酸性(水溶液):HSCN > H2CO3 > HCN |
金属-硫电池价格低廉,使用寿命较长,能量密度高,因而在电池研究领域得到广泛关注。最近,我国科研工作者研究了一种能在室温下工作的新型Na-S电池。该电池放电过程的总反应方程式如下:nS + 2Na = Na2Sn
注:能量密度指单位质量的电极材料可输出的电能,以W·h·kg-1为计量单位。
则下列说法不正确的是( )
| A.该电池中用固态金属Na为负极,S单质作为正极,但S单质须负载在导电材料上 |
| B.该电池的电解质必须具备室温下传导Na+的能力,但不宜用NaOH溶液作为电解液 |
| C.n值越大则该电池的能量密度越高 |
| D.该电池充电过程中阳极的电极反应式:Na2Sn-2e-=2Na++ nS,故充电时Na+从阳极向阴极迁移 |
下列有关作用力的说法正确的是( )
| A.金属键、离子键、分子间作用力、氢键都没有方向性和饱和性 |
| B.键能、金属的原子化热、晶格能分别可以衡量氢键、金属键、离子键的强弱 |
| C.离子键、金属键、氢键、范德华力本质上都是静电作用 |
| D.乙酸、丙醇、丙酮的沸点都比丁烷高是因为前三者分子间都存在氢键 |
设NA表示阿伏加德罗常数(约为6.02×1023mol-1 ),下列有关叙述不正确的是( ) ①在标准状况下,VL水含有的氧原子个数为
①在标准状况下,VL水含有的氧原子个数为
 ②常温常压下,1mol碳烯(:CH2)所含电子总数为8NA
②常温常压下,1mol碳烯(:CH2)所含电子总数为8NA ③1L pH=1的水溶液中,水合氢离子数为0.1NA
③1L pH=1的水溶液中,水合氢离子数为0.1NA ④1molOH-在电解过程中被氧化,提供电子的数目为NA个
④1molOH-在电解过程中被氧化,提供电子的数目为NA个 ⑤22.4L的HCl溶于水,溶液中H+数为NA
⑤22.4L的HCl溶于水,溶液中H+数为NA ⑥1 mol CO2与含2 mol NaOH的溶液反应后,溶液中CO32-数为NA
⑥1 mol CO2与含2 mol NaOH的溶液反应后,溶液中CO32-数为NA ⑦12g金刚石中所含共价键数目为NA
⑦12g金刚石中所含共价键数目为NA ⑧Na2O2与H2O反应,生成常温常压下16gO2,反应中转移电子数为NA
⑧Na2O2与H2O反应,生成常温常压下16gO2,反应中转移电子数为NA ⑨标准状况下,2.24L苯中约含有3.612 x 1023个碳原子
⑨标准状况下,2.24L苯中约含有3.612 x 1023个碳原子 ⑩25℃时,1 L pH=13的氢氧化钠溶液中约含有6.02×l023个氢氧根离子
⑩25℃时,1 L pH=13的氢氧化钠溶液中约含有6.02×l023个氢氧根离子
| A.①②③④ | B.⑤⑥⑦⑧⑨ | C.①⑤⑥⑦⑨⑩ | D.③⑤⑥⑧⑨⑩ |