下列都是用盐酸来制取氯气的反应,为了制得等量的氯气,起还原作用的盐酸用量最少的是()
A.MnO2+4HCl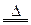 MnCl2+Cl2↑+2H2O MnCl2+Cl2↑+2H2O |
B.2KMnO4+16HCl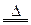 2KCl+2MnCl2+5Cl2↑ 2KCl+2MnCl2+5Cl2↑ |
C.KClO3+6HCl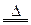 KCl+3Cl2↑+3H2O KCl+3Cl2↑+3H2O |
D.2HCl(aq)  H2↑+Cl2↑ H2↑+Cl2↑ |
常温时,下列各组离子能大量共存的是( )
| A.Ag+、K+、NO3-、Cl- | B.Fe3+、NH4+、SO42-、NO3- |
| C.Fe2+、Na+、Cl-、ClO- | D.H+、I-、SO42-、HCO3- |
下列各组物质不能按“
 ”所示关系实现转化的是(“
”所示关系实现转化的是(“
 ”表示反应一步完成)
”表示反应一步完成)
A. |
B. |
C. |
D.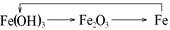 |
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.160gBr2所含原子数目为2NA |
| B.在标准状况下,22.4L水的物质的量是1mol |
| C.22.4L氯化氢溶于水可电离出1molCl- |
| D.在常温常压下,11.2L氧气含有的分子数为0.5NA |
下列物质的用途中利用了氧化还原反应原理的是
| A.用明矾净水 | B.用“84消毒液(有效成分为NaClO)”消毒 |
| C.用食盐腌渍食物 | D.用小苏打治疗胃酸过多 |
下列有关化学用语使用正确的是
| A.39Ca与40Ca互为同位素 |
B.中子数为18的氯原子结构示意图: |
C.用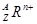 表示某微粒,则其所含质子数为A-n 表示某微粒,则其所含质子数为A-n |
D.NaHCO3在水溶液中的电离方程式:NaHCO3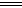 Na++H++CO32- Na++H++CO32- |