1956年,杨振宁和李政道提出在弱相互作用中宇称不守恒,并由吴健雄用 放射源进行了实验验证。次年,杨振宁、李政道两人因此获得诺贝尔物理奖。
放射源进行了实验验证。次年,杨振宁、李政道两人因此获得诺贝尔物理奖。 的衰变方程为:
的衰变方程为: ====
====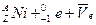
其中,Ve是反中微子,它的电荷为零,静止质量可认为是零。
(1)下列关于 的叙述,错误的是_______________。
的叙述,错误的是_______________。
A.质子数是27 B.电子数是27
C.质量数是27 D.中子数是60
(2)CO与Fe同周期,它位于元素周期表的第_______________周期,第______________族。
(3)在上述衰变方程中,衰变产物Ni的质量数A为_______________,核电荷数Z为_______________。
(4)元素的化学性质主要决定于_______________。
A.核外电子数 B.核内质子数
C.核内中子数 D.最外层电子数
(5)不同种元素的本质区别是_______________。
A.质子数不同 B.中子数不同
C.电子数不同 D.质量数不同
下列关干氧化物的各项叙述正确的是
①酸性氧化物不一定是非金属氧化物
②非金属氧化物肯定是酸性氧化物
③碱性氧化物肯定是金属氧化物
④金属氧化物肯定是喊性氧化物
⑤酸性氧化物均可与水反应生成相应的酸
⑥与水反应生成酸的氧化物不一定是酸性氧化物,与水反应生成碱的氧化物不一定是碱住氧化物
⑦不能跟酸反应的氧化物一定能跟碱反应
| A.①③⑥ | B.①②⑤⑦ | C.③④⑤ | D.①②⑤ |
下列离子方程式正确且与对应实验相符合的是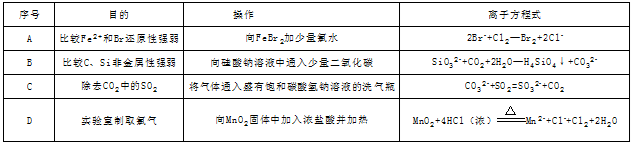
化学方程式可简明地体现元素及其化合物的性质。
已知: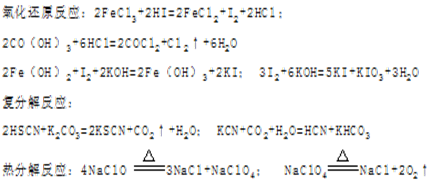
下列说法不正确是:
| A.酸性(水溶液):HSCN〉H2CO3〉HCN |
| B.还原性(碱性溶液):Fe(OH)2〉I—〉KIO3 |
| C.热稳定性:NaCl〉NaClO4〉NaClO |
| D.氧化性(酸性溶液):I2〉FeCl3〉Co(OH)3 |
工业上用的铝上矿(主要成分是氧化铝.含氧化铁杂质)为原料冶炼铝的工艺流程如下:
下列叙述正确的是
| A.反应①中试剂X是氢氧化钠溶液 |
| B.试剂Y是HCI,它与AlO2-反应生成氢氧化铝 |
| C.图中所示转化反应中包含2个氧化还原反应 |
| D.将X与Y试剂进行对换,最终可以达到相同结果 |
将a气体通人BaCl2溶液中,没有沉淀生成.然后再通人b气体,有沉淀生成,则a,b不可能
| A.a是Cl2,b是CO2 | B.a是SO2,b是H2S |
| C.a是NH3,b是CO2 | D.a是SO2,b是Cl2 |