实验室要配制2.0 mol·L-1 KNO3溶液100 mL,不使用的化学仪器是( )
①烧杯 ②250 mL容量瓶 ③100 mL容量瓶 ④玻璃棒 ⑤胶头滴管 ⑥托盘天平
| A.只有② | B.②⑥ | C.①③ | D.①④ |
有如下两个反应(反应所需的其他条件和各物质的化学计量数均已略去):
①X+Y Z+P+Q;②Z+Q
Z+P+Q;②Z+Q X+H+Y。请针对以下两种不同情况来完成:
X+H+Y。请针对以下两种不同情况来完成:
(1)若X是一种日常生活中用作调味剂的盐,反应①是化学工业上制取单质Q和化合物Z的重要方法。则Z的电子式为___________________;反应①中阴极反应为___________________;反应②的离子方程式为______________;在酸性条件下,若将化合物H加到含Fe2+的溶液中,溶液从浅绿色变成黄色,该反应的离子方程式为_______________________________________。
(2)若X是一种含氧酸盐,可用于实验室中检验水的存在。1个X的酸根离子中共含有50个电子,其中含有一种元素R,R的原子最外层电子数是电子层数的2倍,则R在元素周期表中的位置是_________。X单质的熔点是112.8 ℃,则R单质的晶体类型属于______晶体。
(3)若X是(2)中的含氧酸盐,当以石墨作电极电解X溶液时,阳极反应为___________________;原溶液体积为1升,C(H+)=1×10-6mol/L。电解一段时间,当阳极收集到56ml(标况下)气体是,假定溶液体积不变,阴极棒将增重______g,此时电解质溶液的PH为_____。
某校课外实验小组进行铜与浓、稀硝酸反应的实验研究。基本原则是:安全可靠、现象明显,符合环保要求。
如果用图Ⅰ中装置进行铜与浓硝酸反应的实验,最大缺点是产生的NO2气体逸出污染空气;如果用该装置来证明铜与稀硝酸反应生成NO气体,缺点是不易观察到有毒性的NO气体无色的本来面目。
(1)若用装置Ⅱ进行实验,既可克服实验不足,还能使上述反应在同一试管中连续进行。实验如下:组装好装置并检查气密性后,加入2 mL浓硝酸(铜片未接触酸液),塞紧胶塞;向左倾斜试管使其反应发生,当导管口有极少量红棕色气体逸出,溶液呈绿色时,正立试管,使反应停止;同时将导管插入水中,稍后能观察到:a.水沿导管倒吸至试管中,b.________________,c. ________________等明显现象。其中发生的原因用方程式表示为:_________________________________________________________。
(2)当试管中液体体积约占1/2时,从水中取出导管,并伸入一小试管中,管口塞上浸有碱液的棉花(如图Ⅲ)。这样做的目的是:________________,此时大试管中反应的离子方程式为:________________________________________________。
(3)若用右上图Ⅳ所示的装置(U形管、干燥管、A为活塞)制取NO可能更加理想。请补充下列实验步骤:
①检查装置的气密性的方法是:________________________________________________。
②打开活塞A,从U形管右端注入稀硝酸,直到________________________为止。
③关闭活塞A,若反应缓慢,可在U形管左侧加热,观察到____________________。
(6分)有一瓶澄清的溶液,其中可能含有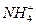 、K+、Na+、Mg2+、Ba2+、Al3+、Fe2+、
、K+、Na+、Mg2+、Ba2+、Al3+、Fe2+、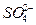 、
、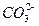 、
、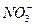 、Cl-、Al O2-、I-,取该溶液进行如下实验:
、Cl-、Al O2-、I-,取该溶液进行如下实验:
(1)用pH试纸实验,表明溶液呈强碱性,焰色反应透过蓝色钴玻璃观察到紫色火焰。
(2)取部分溶液,加入少量CCl4及数滴新制的氯水,经摇荡后,CCl4层呈紫红色。
(3)另取部分溶液,逐滴加入稀HCl溶液,使溶液从碱性逐渐变为酸性,在滴加过程中溶液出现沉淀。滴加完毕后,溶液中沉淀消失。
(4)取部分上述酸性溶液,加BaCl2溶液,有白色沉淀生成。
(5)往(3)得到的酸性溶液通H2S气体,溶液中有浅黄色沉淀产生。
根据上述实验事实确定并完成下列问题:
在溶液中肯定存在哪些离子_________________________________________,
肯定不存在哪些离子_______________________________________________,
还不能确定存在哪些离子___________________________________________。
某品牌消毒液包装说明的部分内容摘录如下:主要有效成份为次氯酸钠,有效氯含量8000-10000mg/L。可用于各类家居用品、餐具、棉织衣物等的消毒,对彩色织物可能有褪色作用。切勿用于丝绸、毛、尼龙、皮革、油漆表面,勿用于铝、铜、碳钢制品。本品须密封,置阴凉暗处保存。请完成以下实验探究过程:
1.阅读材料,获取信息
(1)推测该消毒液的酸碱性: ,原因是(用离子方程式表示) 。
(2)该消毒液还具有的化学性质是 性和 性。
(3)从该消毒液的保存要求分析,导致其失效的外界因素主要是 。
2.确定要研究的问题
该消毒液对碳钢制品是否有腐蚀作用?
3.设计方案,实施探究
用烧杯取少量样品,将一颗光亮的铁钉放入烧杯,浸泡一段时间。对可能产生的现象有如下假设:
假设①:有明显现象;假设②:无明显现象。
(4)基于假设①,结论是铁钉被腐蚀,预期的实验现象是 。
(5)基于假设②,结论是 ,请设计实验进一步验证该结论,叙述实验操作: 。
(8分)实验员不慎忘了给新配制的溶液贴标签,只知道这四瓶液体是:蛋白质溶液、淀粉溶液、淀粉酶溶液和蒸馏水。现有碘试剂和三氯乙酸(会使蛋白质变性,蛋白质溶液变浑浊),请你用这两种试剂,以最佳方法和步骤区分四种未知溶液。