X、Y、Z是主族元素的单质,K、H是化合物,它们有如下关系(式中各物质的化学计量数和反应条件已略去):
(1)①X+K H+Y ②X+Z
H+Y ②X+Z H ③Y+Z
H ③Y+Z K
K
若X和Y的组成元素是同一主族,请写出符合①式的三个不同的化学方程式,并配平:___________________, __________________,__________________。
若X和Y的组成元素不是同一主族,请写出符合①式的3个不同的化学方程式,并配平(3个式子中的3种X和3种Y,分别由不同的元素组成):__________,__________,__________。
(2)今有某化合物W,它跟化合物K或CO2反应,都能生成单质Y。符合该条件(题设的3个“通式”)的单质X是__________,单质Y是__________,单质Z是__________,化合物W是__________。(均写出化学式)
有a、b、c、d、f五种前四周期元素,原子序数依次增大,a、b、c三种元素的基态原子具有相同的能层和能级,第一电离能I1(a)<I1(c)<I1(b)且其中基态b原子的2p轨道处半充满状态,已知bc2+与ac2互为等电子体,d为周期表前四周期中电负性最小的元素,f的原子序数为29。请回答下列问题。(如需表示具体元素请用相应的元素符号)
(1)写出bc2+的电子式__________,基态f原子的核外电子排布式为___________。
(2)b的简单氢化物极易溶于c的简单氢化物,其主要原因是。
(3)化合物甲由c、d两种元素组成,其晶胞如甲图,甲的化学式___________。
(4)化合物乙的部分结构如乙图,乙由a、b两元素组成,硬度超过金刚石。①乙的晶体类型为________________________,其硬度超过金刚石的原因是_________________________。
②乙的晶体中a、b两种元素原子的杂化方式均为___________________。
最近,我国利用生产磷铵排放的废渣磷石膏制取硫酸并联产水泥的技术研究获得成功。具体生产流程如图: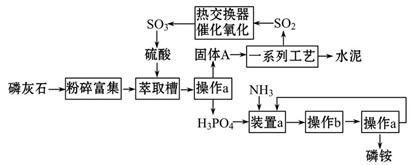
回答下列问题:
(1)操作a的名称是___________,实验室中进行此操作的非玻璃仪器或用品有________________;在实验室中操作b的名称是______________________。
(2)装置a中生成两种酸式盐,它们的化学式分别是_______________。
(3)依题意猜测固体A中一定含有的物质的化学式是____________________(结晶水部分不写)。
(4)热交换器是实现冷热交换的装置。化学实验中也经常利用热交换来实现某种实验目的,气、液热交换时通常使用的仪器是________________________。
(5)制硫酸所产生的尾气除了含有N2、O2外,还含有SO2,微量的SO3和酸雾。能用于测定硫酸尾气中SO2含量的是___________________。
| A.NaOH溶液、酚酞试液 | B.KMnO4溶液、稀硫酸 |
| C.碘水、淀粉溶液 | D.氨水、酚酞试液 |
运用化学反应原理知识在工业生产中有重要意义。
(1) 工业生产可以用NH3(g)与CO2(g)经两步反应生成尿素,两步反应的能量变化示意图如下:
则NH3(g)与CO2(g)反应生成尿素的热化学方程式为________________。
(2)工业生产中用CO可以合成甲醇CO(g)+2H2(g)  CH3OH(g),ΔH=-90.1 kJ·mol-1在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示。
CH3OH(g),ΔH=-90.1 kJ·mol-1在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示。
①p1________p2(填“大于”、“小于”或“等于”);
②100 ℃时,该反应的化学平衡常数K=_____(mol·L-1)-2;
③在其它条件不变的情况下,再增加a mol CO和2a molH2,达到新平衡时,CO的转化率________(填“增大”、“减小”或“不变”)。
(3)工业生产中用SO2为原料制取硫酸
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触。请写出该电池的负极的电极反应式_______________。
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸。电解原理示意图如下图所示。请写出开始时阳极反应的电极反应式__________。
(4)工业生产中用氨水吸收SO2
若将等物质的量的SO2与NH3溶于水充分反应,写出该反应的离子方程式,所得溶液呈性。
(14分)X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号)
(2)X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质(写分子式)
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系
其中C是溶于水显酸性的气体;D是淡黄色固体。
写出C的结构式;D的电子式。
①如果A、B均由三种元素组成,B为两性化合物,且不溶于水,则由A转化为B的离子方程式为。
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因。
A、B浓度均为0.1mol/L等体积的混合溶液中,离子浓度由大到小的顺序为。
依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题: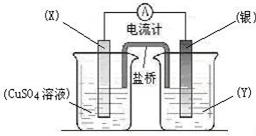
(1)电极X的材料是 (化学式);电解质溶液Y是;
(2)银电极为电池的极,发生的电极反应为;X电极上发生的电极反应为;
(3)外电路中的电子是从电极流向电极。