1,2 - 二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃ ,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验室中可以用下图所示装置制备1,2- 二溴乙烷,其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。填写下列空白:
,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验室中可以用下图所示装置制备1,2- 二溴乙烷,其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。填写下列空白: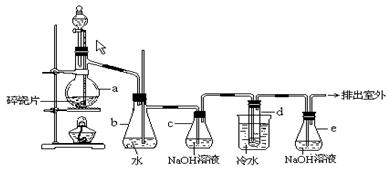
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式.
_________________________;______________________________ ______;
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象._______________________________________________________;
(3)容器c中NaOH溶液的作用是:__________________________________;
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫 酸混合液的量比正常情况下超过许多,如果装置的气密性没有问题,试分析其可能的原因:________ _______________________;_______________________。
酸混合液的量比正常情况下超过许多,如果装置的气密性没有问题,试分析其可能的原因:________ _______________________;_______________________。
(11分) 已知乙醇可以和氯化钙反应生成微溶于水的CaCl2·6C2H5OH。有关的有机试剂的沸点如下:CH3COOC2H5 77.1℃ C2H5OC2H5(乙醚) 34.5℃ C2H5OH 78.3℃ CH3CO
78.3℃ CH3CO OH 118℃实验室合成乙酸乙酯粗产品的步骤如下:在蒸馏烧瓶内将过量的乙醇与少量浓硫酸混合,然后经分液漏斗边滴加醋酸、边加热蒸馏。得到含有乙醇、乙醚、醋酸和水的乙酸乙酯粗产品。
OH 118℃实验室合成乙酸乙酯粗产品的步骤如下:在蒸馏烧瓶内将过量的乙醇与少量浓硫酸混合,然后经分液漏斗边滴加醋酸、边加热蒸馏。得到含有乙醇、乙醚、醋酸和水的乙酸乙酯粗产品。
(1)写出合成乙酸乙酯的反应原理:____________________________________________。
(2)反应中加入乙醇是过量的,其目的是:。
将粗产品再经下列步骤精制:
(3)为除去粗产品其中的醋酸,可向产品中加入__________(填字母)。
A.无水乙醇 B.碳酸钠粉末 C.无水醋酸钠
(4)再向其中加入饱和氯化钙溶液,振荡。其目的是: 。
。
(5)最后,将经过上述处理后的液体放入另一干燥的蒸馏瓶内,再蒸馏。蒸馏时,需要的玻璃仪器有:酒精灯、温度计、冷凝管、锥形瓶、尾接管和____________。冷凝管的水流方向为进出,弃去低沸点馏分,收集76—78℃沸程之间的馏分即得。
上网查阅有关煤的干馏资料,并根据下图所示煤的干馏实验,完成下列问题:
(1)指出图中各仪器的名称:
a________________,b_________________,c_________________,d_________________。
(2)装置c的作用是_________________,d中液体有_________________和_________________。其中的有机物里溶有_________________,可用_________________检验出来;有机物可通过_________________方法使其中的重要成分分离出来。
(3)e处点燃的气体是_________________,火焰是_________________色。
( 6分)如右图。在一支试管中放入一小块铜片,再加入少量浓硫酸,然后把试管固定在铁架台上。把一小条蘸有品红溶液的滤纸放入带有单孔橡皮塞的玻璃管中。塞紧试管口,在玻璃导管口处缠放一团蘸有Na2CO3溶液的棉花。给试管加热,观察现象。当试管中的液体逐渐透明时,停止加热。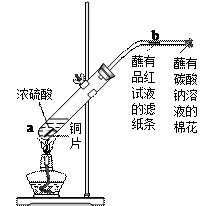
回答下列问题:
(1)试管中的液体反应一段时间后,b处滤纸条的变化为_。
待试管中反应停止后,给玻璃管放有蘸过品红溶液的滤纸处微微加热,滤纸条的变化为。
(2)待试管中的液体冷却后,将试管上层液体倒去,再慢慢加入少量水,可观察溶液呈色。
(3)玻璃导管口蘸有Na2CO3溶液的棉花所起的作用是,有关反应的化学方程式为。
“碘钟”实验中,3I-+S2O===I+2SO的反应速率可以用I与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:
| 实验编号 |
① |
② |
③ |
④ |
⑤ |
| c(I-)/(mol·L-1) |
0.040 |
0.080 |
0.080 |
0.160 |
0.120] |
| c(S2O)/(mol·L-1) |
0.040 |
0.040 |
0.080 |
0.020 |
0.040 |
| t/s |
88.0 |
44.0 |
22.0 |
44.0 |
t1 |
回答下列问题:
(1)该 实验的目的是_____________________________________________________。
实验的目的是_____________________________________________________。
(2)显色时间t1=____________________________ (3)温度
(3)温度 对该反应的反应速度的影响符合一般规律,若在40℃下进行编号③对应浓度的
对该反应的反应速度的影响符合一般规律,若在40℃下进行编号③对应浓度的 实验,显色时间t2的范围为__________(填字母)。
实验,显色时间t2的范围为__________(填字母)。
| A.<22.0 s | B.22.0 s~44.0 s |
| C.>44.0 s | D.数据不足,无法判断 |
(4)通过分析比较上表数据,得到的结论是____________。