有如下两个反应(反应所需的其他条件和各物质的化学计量数均已略去):
①X+Y Z+P+Q;②Z+Q
Z+P+Q;②Z+Q X+H+Y。请针对以下两种不同情况来完成:
X+H+Y。请针对以下两种不同情况来完成:
(1)若X是一种日常生活中用作调味剂的盐,反应①是化学工业上制取单质Q和化合物Z的重要方法。则Z的电子式为___________________;反应①中阴极反应为___________________;反应②的离子方程式为______________;在酸性条件下,若将化合物H加到含Fe2+的溶液中,溶液从浅绿色变成黄色,该反应的离子方程式为_______________________________________。
(2)若X是一种含氧酸盐,可用于实验室中检验水的存在。1个X的酸根离子中共含有50个电子,其中含有一种元素R,R的原子最外层电子数是电子层数的2倍,则R在元素周期表中的位置是_________。X单质的熔点是112.8 ℃,则R单质的晶体类型属于______晶体。
(3)若X是(2)中的含氧酸盐,当以石墨作电极电解X溶液时,阳极反应为___________________;原溶液体积为1升,C(H+)=1×10-6mol/L。电解一段时间,当阳极收集到56ml(标况下)气体是,假定溶液体积不变,阴极棒将增重______g,此时电解质溶液的PH为_____。
(16)某课外活动小组设计了以下实验方案验证Cu与浓硝酸反应的过程中可能产生NO。其实验流程图如下:
(1)测定硝酸的物质的量
反应结束后,从下图B装置中所得100mL溶液中取出25.00mL溶液,用0.1mol·L-1的NaOH溶液滴定,用酚酞作指示剂,滴定前后的滴定管中液面的位置如右上图所示。在B容器中生成硝酸的物质的量为mol。
(2)测定NO的体积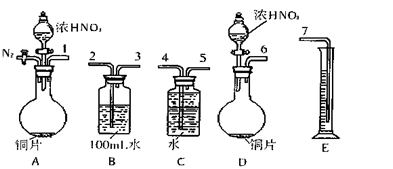
①从上图所示的装置中,你认为应选用装置进行Cu与浓硝酸反应实验,选用的理由是。
②选用上图所示仪器组合一套可用来完成实验并测定生成NO体积的装置,其合理的连接顺序是(填各导管口编号)。
③在测定NO的体积时,若量筒中水的液面比集气瓶的液面要低,此时应将量筒的位置
(“下降”或“升高”),以保证量筒中的液面与集气瓶中的液面持平。
(3)气体成分分析:若实验测得NO的体积为112.0mL(已折算到标准状况),则Cu与浓硝酸反应的过程中(填“有”或“没有”)NO产生,作此判断的依据是。
(4)实验前,用托盘天平称取的铜片至少应为g。
A、B、C、D、E五种可溶性化合物,分别由阳离子Fe3+、Ba2+、Al3+、Na+、Ag+和阴离子NO3-、OH-、SO42-、Cl-、CO32-中的各一种组成(离子不重复)。现做如下实验:
|
①A和E的溶液显碱性,0.1mol·L-1A溶液的pH小于13;
②在B的溶液中逐滴加入氨水有白色沉淀生成,继续加氨水至过量,沉淀消失下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。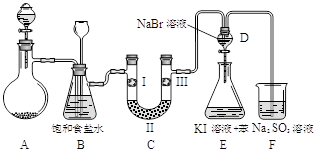
⑴制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为:
__________________________________________________________________。
⑵装置B中饱和食盐水的作用是_______________;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象______________________________。
⑶装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入_______。
| a |
b |
c |
d |
|
| I |
干燥的有色布条 |
干燥的有色布条 |
湿润的有色布条 |
湿润的有色布条 |
| II |
碱石灰 |
硅胶 |
浓硫酸 |
无水氯化钙 |
| III |
湿润的有色布条 |
湿润的有色布条 |
干燥的有色布条 |
干燥的有色布条 |
⑷设计装置D、E的目的是比较氯、溴、碘的非金属性。当向D中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为______色,说明氯的非金属性大于溴。
⑸打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是_____________。
⑹有人提出,装置F中可改用足量的NaHSO3溶液吸收余氯,试写出相应的离子反应方程式:
______________________,判断改用NaHSO3溶液是否可行______(填“是”或“否”)。
(16分)某学习小组以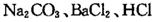 溶液作试剂,设计提纯含有少量
溶液作试剂,设计提纯含有少量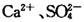 的粗盐。其实验方案如下:
的粗盐。其实验方案如下: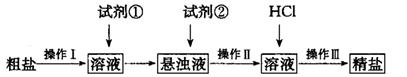
(1) 操作I的名称为________;试剂①应选用_______;检验试剂②是否过量的方法______。
(2) 操作I〜III共用到玻璃棒________次;从悬浊液到精盐的实验过程中,某同学未按上述方案进行,最终导致精盐纯度偏低。其做法可能是________________。
(3)测定产品精盐中NaCl的含量的实验步骤是:
第一步:准确称取a g干燥精盐于锥形瓶中,加人30. OmL蒸馏水。
第二步:向上述锥形瓶中加人几滴突光素指示剂。
第三步:用浓度为的AgNO3标液滴至终点(溶液呈浅红色),消耗AgNO3溶液V mL。
①盛装干燥精盐的烧杯应放在________中保存(填仪器名称);
②终点时溶液呈浅红色是荧光素指示剂与________反应(填“Ag+”或"NO3-”);
③某同学在第二次滴定时,滴定前,后管内液面分别如图,则其所得V=________mL;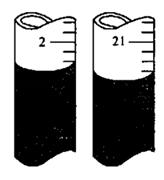
④NaCl的质量分数为________ (用字母表示)
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有;
(2)硫酸铜溶液可以加快氢气生成速率的原因是;
(3)实验室中现有
、
、
、
等4种溶液,可与实验中
溶液起相似作用的是;
(4)要加快上述实验中气体产生的速率,还可采取的措施有(答两种);
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量
粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
| 实验 混合溶液 |
||||||
| 4 | 30 |
1 |
2 |
3 |
4 |
5 |
| 饱和 溶液/ | 0 |
0.5 |
2.5 |
5 |
6 |
20 |
|
7 |
8 |
9 |
10 |
10 |
0 |
①请完成此实验设计,其中:
1=,
6=,
9=;
②反应一段时间后,实验
中的金属呈色,实验E中的金属呈色;
③该同学最后得出的结论为:当加入少量
溶液时,生成氢气的速率会大大提高。但当加入的
溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因。