硫酸亚铁是一种可用于治疗缺铁性贫血的药剂,硫酸亚铁药片外表包有一层特制的糖衣,以保护硫酸亚铁不被空气中的O2氧化成硫酸铁。请设计一种方法,验证某硫酸亚铁药品是否已被氧化。请写出主要步骤、现象及化学方程式。
用质量分数为98%,密度为1.84g· cm-3的浓硫酸配制250mL物质的量浓度为2mol·L-1的稀硫酸。
(1)需要使用的主要仪器有量筒、烧杯、玻璃棒、、。
(2)其操作步骤可分解为以下几步:
A.用量筒量取mL浓硫酸,(简述浓硫酸的稀释操作),冷却
B.用蒸馏水洗涤烧杯和玻璃棒2~3次,将每次的洗涤液都转移入容量瓶里
C.将稀释后的硫酸小心地用玻璃棒引流至容量瓶里
D.检查250mL容量瓶是否漏水
E.将蒸馏水直接加入容量瓶至刻度线以下2cm处
F.盖紧瓶塞,上下倒转摇匀溶液
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,到凹液面最低点恰好与刻度线相切
请据此填写:
①完成上述步骤中的空白处。
②正确的操作顺序是(用字母填写):
()→( )→( )→ B →( )→()→()
③进行A步操作时,选用量筒的规格是。(选填字母)
A.10mL B.50mLC.100mL D.1000mL
④下列情况对所配制的稀硫酸浓度有何影响?(选填“偏高”、“偏低”、“无影响”)。
A.用量筒量取浓硫酸时仰视,配制的稀硫酸浓度将
B.容量瓶用蒸馏水洗涤后残留有少量的水_________
C.定容时仰视溶液的凹液面 _________
在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
| 成分 |
质量(g) |
摩尔质量(g ·mol-1) |
| 蔗糖 |
25.00 |
342 |
| 硫酸钾 |
0.25 |
174 |
| 阿司匹林 |
0.17 |
180 |
| 高锰酸钾 |
0.25 |
158 |
| 硝酸银 |
0.02 |
170 |
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是________。
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为_______ mol/L。(注意:只要求用原始数据写出数学表达式,不需要化简与计算)
(3)配制上述“鲜花保鲜剂”所需的仪器有:电子天平、药匙、烧杯、量筒、玻璃棒、______________、_______________。(在横线上填写所缺仪器的名称)
(4)在溶液配制过程中,下列操作对配制结果没有影响的是___________。
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题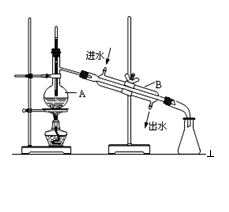
(1)图中明显的两处错误是
①_________________________________________
②_________________________________________
(2)A仪器的名称是______________,B仪器的名称是_______________。
(3)实验时A中除加入自来水外,还需加入少量__________,其作用是________________。
现拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2)。已知实验中可能会发生下列反应:
①2Mg+O2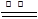 2MgO;②3Mg+N2
2MgO;②3Mg+N2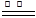 Mg3N2;③2Mg+CO2
Mg3N2;③2Mg+CO2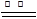 2MgO+C;
2MgO+C;
④Mg+H2O MgO+H2↑; ⑤Mg3N2 +6H2O
MgO+H2↑; ⑤Mg3N2 +6H2O 3Mg(OH)2+2NH3↑
3Mg(OH)2+2NH3↑
可供选择的装置和药品如下图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连)。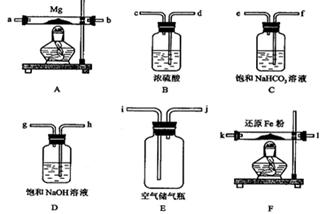
回答下列问题:
(1)在设计实验方案时,除装置A、D、E外,还应选择的装置有(填字母代号),选择装置D目的为_____________________________;
(2)通气后,应先点燃处的酒精灯;如果同时点燃A、F装置的酒精灯,将会使实验结果(填“偏高”或“偏低”)原因
(3)请设计一个实验,验证产物是Mg3N2,写出操作步骤、现象和结论:
_____________________________________________________________________
海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验: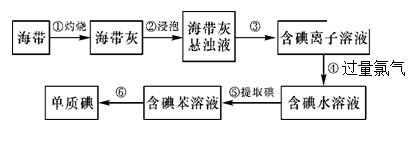
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是
A.烧杯 B.表面皿 C.坩埚 D.酒精灯 E.圆底烧瓶
(2)请写出步骤④中反应的离子方程式:
(3)步骤⑥是从含碘的苯溶液中分离出单质碘和回收苯,还需经过蒸馏,指出并改正下列实验装置中的错误之处(至少两处)。
①
②
(4)步骤⑤中,某学生选择用苯来提取碘,其验操作可分解为如下几步:
(A)把盛有溶液的分液漏斗放在铁架台的铁圈中;
(B)把50毫升碘水和15毫升苯加入分液漏斗中,并盖好玻璃塞;
(C)检验分液漏斗活塞和上口的玻璃塞是否漏液;
(D)倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
(E)旋开活塞,用烧杯接收溶液;
(F)将分液漏斗上口倒出上层溶液;
(G)将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
(H)静置,分层。就此实验,完成下列填空:
①正确操作步骤的顺序是 →→ →A→G→→E→F
②上述(G)步骤操作的目的是
③能选用苯从碘水中萃取碘的原因是