甲、乙两个容器中,分别加入0.1mol/LNaCl溶液与0.1mol/LAgNO3溶液后,以Pt为电极进行电解时,在A、B、C、D各电极上生成物的物质的量之比为:_____________
(7分)能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。
(1)氢气在燃烧时,放出大量热量,说明该反应是_________________热反应,这是由于反应物的总能量____________生成物的总能量;从化学反应的本质角度来看,是由于断裂反应物中的化学键吸收的总能量_______________________形成产物的化学键放出的总能量。
(2)氢气被公认为是21世纪代替矿物燃料的理想能源,5.2 g氢气燃烧时放出286 kJ热量,而每千克汽油燃烧时放出的热量为46000 kJ。试据此分析氢气作为能源代替汽油的优势:_______________________________。
(3)通过氢气的燃烧反应,可以把氢气中蕴含的化学能转化为热能,如果将该氧化还原反应设计成原电池装置,就可以把氢气中蕴含的化学能转化为电能,下图就是能够实现该转化的装置,被称为氢氧燃料电池。该电池的正极是____________ (填“a电极”或“b电极”),在负极发生的电极反应是_________________,
(5分)下列各组组物质中,属于同位素的是(1)_______;属于同素异形体的是(2)____;
互为同分异构体的是(3)_____;属于同系物的是(4)______;属于同种物质的是(5)______。
| A.O2和O3 | B.CH3CH2CH2CH3和CH3CH(CH3)2 | C.35Cl和37Cl | D.CH3(CH2)3CH3和CH3CH3 |
E .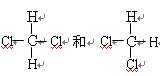
有机物A(C6H8O4)为食 品包装纸的常用防腐剂。A可以使溴水褪色。A难溶于水,但在酸性条件下可发生水解反应,得到B(C4H4O4)和甲醇。通常状况下B为无色晶体,能与氢氧化钠溶液发生反应。
品包装纸的常用防腐剂。A可以使溴水褪色。A难溶于水,但在酸性条件下可发生水解反应,得到B(C4H4O4)和甲醇。通常状况下B为无色晶体,能与氢氧化钠溶液发生反应。
(1)A可以发生的反应有(选填序号)。
①加成反应②酯化反应③加聚反应④氧化反应
(2)B分子所含官能团的名称是。
(3)B分子中没有支链,其结构简式是,B的具有相同官能团 的同分异构体的结构简式是。
的同分异构体的结构简式是。
(4)由B制取A的化学方程式是。
(5)天门冬氨酸(C4H7NO4)是组成人体蛋白质的氨基酸之一,可由B通过以下反应制取:
天门冬氨酸的结构简式是。
化合物A由周期不同的短周期元素X、Y组成,是良好的耐热冲击材料。
(1)X的单质既可与盐酸反应,又可与NaOH溶液反应,X的原子结构示意图为 。
(2)X的硫酸盐溶液与过量NaOH溶液反应的离子方程式为
(3)一定条件下,A和水缓慢作用生成含Y的化合物Z,Z分子含有10个电子。
①Z与H2O2反应,其产物之一是Y的单质,单质Y的电子式为 ;Z分子的空间结构呈。 ②A的化学式是
;Z分子的空间结构呈。 ②A的化学式是
(4)X的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用),其反应的化学方程式是

现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子 Na+、Al3+、Mg2+、Ba2+、Fe3+和五种阴离子Cl-、OH-、NO3-、CO32-、X中的一种。
(1)某同学通过比较分析,认为无需检验就可判断其中必有的两种物质是和_______(填化学式)。
(2)为了确定X,现将(1)中的两种物质记为A和B,含X的物质记C,当C与B的溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时产生棕黄色沉淀,向该沉淀中滴人稀硝酸沉淀部分溶解,最后留有白色沉淀不再溶解。则X为____。
A.SO32-B.SO42-C.CH3COO-D.SiO32-
(3)B的水溶液显___性,原因为____。(用离子方程式表示)
(4)将0. 02 molA与0.0 1molC同时溶解在足量的蒸馏水中,充分反应后,最终所得沉淀的质量为________(保留一位小数)。
(5)将Cu投人到装有D溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现。则物质D一定含有上述离子中的_____(填相应的离子符号)。有关反应的离子方程式为:____________。
(6)利用上述已经确定的物质,可以检验出D、E中的阳离子。请简述实验操作步骤、现象及结论_________________。