(14分)化学上常用燃烧法确定有机物组成,这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成,图中所列装置是用燃烧法确定有机物分子式常用的装置。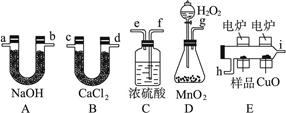
完成下列问题:
(1)产生的氧气按从左到右流向,所选择的装置各导管的连接顺序是________________。
(2)C装置中浓硫酸的作用是__________________。
(3)D装置中MnO2的作用是__________________。
(4)燃烧管中CuO的作用是__________________。
(5)若准确称取0.09 g样品(只含C、H、O三种元素中的两种或三种)经充分燃烧后,A管质量增加13.2 g,B管质量增加0.54 g,则该有机物的实验式为__________________________。
(6)要确定该有机物的分子式,还要_______________。
(12分)某实验小组利用如下图所示装置完成有关实验。
(1) 有关 气体的制取、收集、尾气处理问题
气体的制取、收集、尾气处理问题
①仪器a的名称:__________,若装置I用于制取SO2,则反应的化学方程式为: __________
装置III可用于气体的吸收,若用于吸收Cl2,则IH中所盛放液体为____________________
| A.水 | B.浓硫酸 | C.NaOH溶液 | D.饱和NaCl溶液 |
②装置II可以是收集装置也可以是洗气装置.若用来收集N0,请简述其操作方法:____________________
(2) 比较碳、硅两种元素的非金属性强弱(a中装的盐酸、装置II中装有Na2SiO3溶液)
则装置II中盛放的溶液为____________________
装置III中反应的离子方程式为____________________
如图所示,是一个制取氯气并以氯气为原料进行特定反应的装置,其中各试剂瓶装的试剂为: B(适量澄清石灰水溶液),C(水),E(紫色石蕊试液)。
(1)A是氯气发生装置 ,蒸
,蒸 馏烧瓶中盛放MnO2固体,其化学反应方程式是:。
馏烧瓶中盛放MnO2固体,其化学反应方程式是:。
(2)实验开始时,先点燃A处酒精灯,打开分液漏斗旋塞和Ⅰ处活塞,让氯气充满整个装置,再点燃D处酒精灯,请写出B中的化学方程式
(3)在D装置的硬质玻璃管内盛有碳粉,发生氧化还原反应,一种产物能使E处紫色石蕊试液变红,另一产物能使澄清石灰水变浑浊,写出D中的反应的化学方程式_________。
(4)在E处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是。
(5)D处反应完毕后关闭分液漏斗旋塞,移去酒精灯,但由于余热的作用,A处仍有氯气产生,此时应该怎样操作 ;装置Ⅰ中的现象是。
;装置Ⅰ中的现象是。
(6)若将C中的水换成氢氧化钠溶液,溶液中不但有NaClO还有NaClO3,其物质的量比为2:1,则氧化剂和还原剂的物质的量比为:。
阅读、分析下列两个材料:
材料一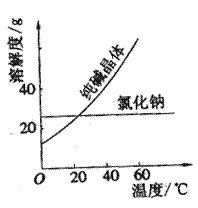
材料二
| 物质 |
熔点/℃ |
沸点/℃ |
密度/g·cm-3 |
溶解性 |
| 乙二醇 C2H6O2 |
-11.5 |
198 |
1.11 |
易溶于水和乙醇 |
| 丙三醇C3H8O3 |
17.9 |
290 |
1.26 |
能跟水、酒精以任意比互溶 |
根据上述材料及课本知识,回答下列问题(填写序号):
A.蒸馏法 B.萃取法 C.“溶解、结晶、过滤”的方法 D.分液法E.层析
⑴将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用______________,
⑵将乙二醇和丙三醇相互分离的最佳方法是______________,
⑶用CCl4提取溴水中的溴单质的最佳方法是_____________,
⑷分离汽油和水的最佳方法是_______________。
有人设计出一种在隔绝空气下让钠与水反应的方法,利用煤油来控制反应速率。使学生能仔细观察到各种实验现象。该方法简便、安全、现象明显、有趣味性。实验装置如图所示,将规格为6×55 mm玻璃管和长颈漏斗插入橡皮孔中,玻璃管外套上30 mm的乳胶管,乳胶管上再接规格为6×30 mm金属尖嘴管,乳胶管上夹上弹簧夹。
实验时,往100 mL的大试管中先加入40 mL煤油,取2粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过漏斗加满滴有酚酞的水。根据反应中观察到的现象,回答下列问题。
根据反应中观察到的现象,回答下列问题:
(1)金属钠变化的现象是_____________
。
(2)大试管中溶液颜色的变化是_______________。
(3)装置中液面的变化分别是:
大试管中_________ ;
;
长颈漏斗中________________。
(4)简述检验产生的气体的方法:______________________。
如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。
(1)图中的两处明显的错误是
①_______________________________________
②_______________________________________
(2)A仪器的名称是_ _____________,
_____________,
B仪器的名称是_______________。
(3)实验时A中除加入自来水外,还需加入少量__________,其作用是________________。