如图所示,是一个制取氯气并以氯气为原料进行特定反应的装置,其中各试剂瓶装的试剂为: B(适量澄清石灰水溶液),C(水),E(紫色石蕊试液)。
(1)A是氯气发生装置 ,蒸
,蒸 馏烧瓶中盛放MnO2固体,其化学反应方程式是: 。
馏烧瓶中盛放MnO2固体,其化学反应方程式是: 。
(2)实验开始时,先点燃A处酒精灯,打开分液漏斗旋塞和Ⅰ处活塞,让氯气充满整个装置,再点燃D处酒精灯,请写出B中的化学方程式
(3)在D装置的硬质玻璃管内盛有碳粉,发生氧化还原反应,一种产物能使E处紫色石蕊试液变红,另一产物能使澄清石灰水变浑浊,写出D中的反应的化学方程式_________。
(4)在E处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是 。
(5)D处反应完毕后关闭分液漏斗旋塞,移去酒精灯,但由于余热的作用,A处仍有氯气产生,此时应该怎样操作  ;装置Ⅰ中的现象是 。
;装置Ⅰ中的现象是 。
(6)若将C中的水换成氢氧化钠溶液,溶液中不但有NaClO还有NaClO3,其物质的量比为2:1,则氧化剂和还原剂的物质的量比为: 。
(15分)某化学兴趣小组利用以下各装置连接成一整套装置,探究氯气与氨气之间的反应.其中D为纯净干燥的氯气与纯净干燥氨气反应的装置.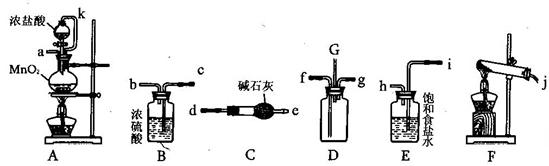
请回答下列问题:
(1)连接好装置后,必需进行的一步实验操作是__________________
(2)装置E的作用是____________,橡胶管k的作用是________________________
(3)从装置D的G处逸出的尾气中可能含有黄绿色的有毒气体,处理方法是__________________
(4)装置F中试管内发生反应的化学方程式____________________________________
(5)接入D装置的两根导管左边较长、右边较短,目的是______________________________
(6)整套装置从左向右的连接顺序是(j)接( ) ( )接(f) (g)接( ) ( )接( ) ( )接(a).
(15分)某研究小组设计如下装置分离CO和CO2的混合气体并探究CO还原氧化铜的产物和过氧化钠的性质。已知氯化钯(PdCl2)溶液遇CO气体会产生黑色沉淀(金属单质)。夹持装置未画出。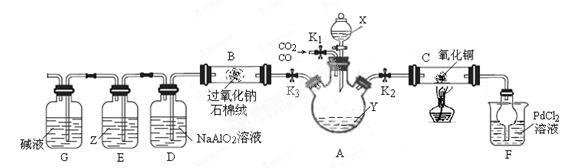
(题9图)
(1)试剂X、Y的焰色反应均呈黄色,则X、Y可能是、.
(2)连接装置、检验气密性并装好药品后,关闭分液漏斗活塞和K3,打开K1、K2,分离出CO,当观察到现象时,可对C装置进行加热操作,反应产物为红色固体。
(3)查询资料获得以下信息:①Cu2O为红色固体;②常温下,Cu2+在溶液中稳定,Cu+易在酸性条件下发生反应:2Cu+ =Cu2++Cu。
甲、乙两组同学取上述红色固体(用M代表)进行实验,探究其成分:
| 组别 |
实验操作 |
实验现象或数据 |
结论 |
| 甲 |
① 向a g M中加入一定量稀硫酸,充分搅拌; ② 继续滴加稀硫酸至过量, 充分反应. |
①固体明显减少; ②仍然有一定量固体,溶液呈蓝色 |
①M中一定有Cu2O; ②M中一定有Cu. |
| 乙 |
将甲实验后所得溶液过滤 将滤渣洗涤、干燥、称量 |
滤渣质量为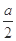 g g |
M为Cu和Cu2O的混合物 |
(i)乙组同学认为甲组同学所得结论不可靠,其理由是.
(ii)甲组同学配合乙组同学进行了计算,认为乙组同学的结论是正确的,并得出M中Cu和Cu2O的物质的量之比是.
(4)C装置反应结束后,欲从混合气体中分离出CO2,需进行的主要操作是.实验过程中D装置产生白色沉淀的离子方程式为.
(5)Z试剂为混有KI的苯溶液,则E装置中可能产生的现象是.
高锰酸钾广泛用作氧化剂、防腐剂、消毒剂、除臭剂及解毒剂。常见的制备流程如下:
已知:a.3MnO2+KClO3+6KOH=3K2MnO4+KCl+3H2O B.3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3
请回答下列问题:
(1)步骤①中反应所选用的坩埚不能用。
A.石英坩埚 B.铁坩埚 C.瓷坩埚 D.石墨坩埚
(2)步骤③通CO2的目的是为了调节溶液的pH,能否改用氯化氢(填“能”或“否”),原因是。
(3)步骤④中抽滤得到的固体是。
(4)抽滤装置主要由、安全瓶、抽气泵和布氏漏斗四部分组成,该实验中抽滤时能否用滤纸?______(填“能”或“不能”), 理由是_____。
(5)从滤液⑤得到高锰酸钾的后续操作步骤是____。
某物质用途广泛,可用作分析试剂、媒染剂、催化剂及化工原料。经测定它含有铁元素,摩尔质量为482g/mol。为进一步确定它的组成,某化学兴趣小组做了以下实验:
Ⅰ.称取48.20g该物质溶于水,配成100mL溶液,所得溶液显棕黄色。
Ⅱ.取上述溶液50mL于试管中,加入足量的0.1mol/LNaOH溶液,并加热,产生的气体经干燥后通入浓硫酸中,浓硫酸增重0.85g;产生的红褐色沉淀经过过滤、洗涤、灼烧后得4.00g固体。
Ⅲ.另取上述溶液50mL于试管中,加入足量的BaCl2溶液,产生不溶于盐酸的白色沉淀 23.30g。
请回答下列问题:
(1)实验Ⅱ中产生气体的电子式。
(2)该物质的化学式为,下列有关该物质的用途合理的是。
| A.补血剂 | B.净水剂 | C.含酚废水的检测试剂 | D.肥料 |
(3)该物质溶液中逐滴加入氢氧化钡溶液至金属元素完全沉淀时的化学反应方程式。
(4)将SO2气体通入该物质的溶液中可以观察到的实验现象是,写出该反应的离子方程式。
(5)为了进一步验证该物质中铁元素的化合价,某同学设计了如下实验方案:取少量固体于试管中,加水充分溶解,滴加硫氰化钾溶液,若溶液显血红色,即可证明该物质中一定存在Fe3+。请评价该实验操作是否合理(填“合理”或者“不合理”),理由。
某校化学兴趣小组的同学设计以下实验来定性检验茶叶中含有钙、铁、铝三种金属元素。【已知完全沉淀的pH:Ca(OH)2:pH ≥ 13;Al(OH)3:pH ≥ 5.5;Fe(OH)3:pH ≥ 4.1】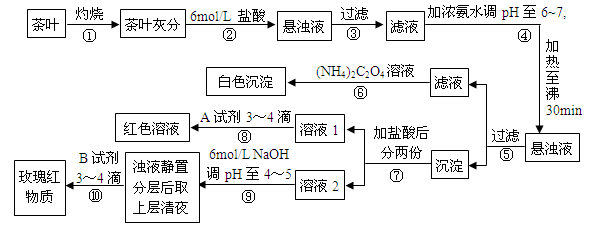
下列说法不正确的是
| A.步骤②加入6mol/L盐酸的主要目的是为了将茶叶灰分中的钙、铁、铝难溶性化合物转化为可溶性氯化物 |
| B.步骤⑤所得滤液中溶质的主要成分为:CaCl2、NH3·H2O |
| C.步骤⑥可以检出钙元素存在,离子反应方程式为Ca2++C2O42- = CaC2O4↓ |
D.步骤⑧中A试剂为KSCN溶液,离子反应方程式为Fe3++3SCN- Fe(SCN)3 Fe(SCN)3 |