(8分)空气中微量的臭氧对人有益,浓度过大则是一种污染气体,臭氧作为强氧化剂,几乎能与任何生物组织反应。
(1)下列有关说法正确的是 ▲ 。
| A.停止使用氟里昂是为保护臭氧层 |
| B.光化学烟雾与大气臭氧的生成有关 |
| C.家用电器消毒柜中产生的臭氧能够高效杀菌消毒 |
| D.臭氧能使湿润的碘化钾-淀粉试纸变蓝 |
(2)臭氧的化学性质极不稳定,在空气和水中都会慢慢分解成氧气,臭氧常用于自来水的消毒,臭氧的溶解度及在水中的分解速度与水温及水的pH关系如下图:
用臭氧消毒自来水,适宜的条件是 ▲ 。
(3)2O3(g) →3O2(g) △H=-285kJ/mol, 2Ag2O(s) =" 4Ag(s)+" O2(g)△H="62.2" kJ/mol,臭氧能与银化合为Ag2O,该反应的热化学方程式为: ▲ 。
(4)臭氧在有机合成有广泛用途,可将烯烃氧化为醛同时生成氧气,试写出2-丁烯与臭氧反应的化学方程式: ▲ 。
I.有机物A是构成营养素的基础物质,A的球棍模型如图所示,图中“棍” 代表单键或双键或三键,不同颜色的球代表不同元素的原子。回答下列问题: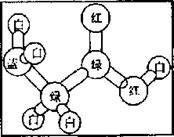
(1)A的分子式是。官能团的名称是 。
(2)下列有关于A的说法中,正确的是 (选填字母);
A.具有两性
B.能发生消去反应
C.不能发生酯化反应
D.名称为甘氨酸
II. A、B、C三种物质的分子式都是C7H8O,若滴入FeCl3溶液,
只有C呈紫色,且C苯环上的一溴代物有两种结构。若投入金
属钠,只有B没有变化。写出A、B、C的结构简式:A__________,B__________,C__________。
III.有机物X (C9H804)是一种应用最早、最广的药物之一,也是重要的合成中间体。有机物X的仪器分析如下: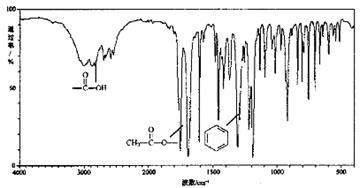
①有机物X的红外光谱
有机物X的核磁共振氢谱图峰面积比是1:1:1:1:3,已知X分子中苯环上只有两个相邻的取代基,则X的结构简式是 。
一份无色溶液中可能含有Na+、Fe3+、H+、Mg2+、CO32﹣、OH﹣、HCO3﹣、Cl﹣、SO42﹣等离子中的若干种。为了确定溶液的组成,进行了如下操作:
①向溶液中滴加酚酞试液,溶液显红色;
②取2mL溶液,先加足量稀硝酸酸化,有气体产生,再加氯化钡溶液进行检验,没有明显现象;
(1)原溶液中一定存在的离子是 ,一定不存在的离是 。
(2)经过上述操作后,还不能肯定是否存在的离子是 。对可能含有的离子,如何进行实验以进一步 。
(3)标准状况下,CO和CO2的混合气体的质量是9.6g,体积是6.72L,则CO2在混合物中的质量分数约为多少?
为了除去粗盐中含有的Ca2+、Mg2+、Fe3+、SO42﹣以及泥沙等杂质,
(1)下列操作正确的顺序是:
①称取粗盐溶解②加过量Na2CO3③加过量NaOH④加过量BaCl2⑤过滤⑥蒸发、结晶、烘干得到 精盐⑦往滤液中加入适量的盐酸
(2)加过量Na2CO3时相关的离子方程式是 。
(3)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是 。
下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题: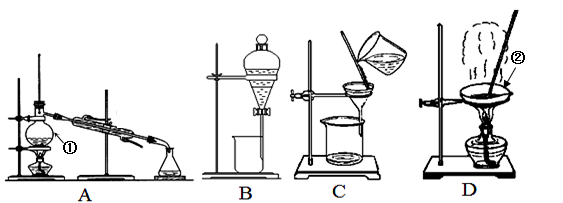
(1)装置A中仪器①的名称是 ,装置D中仪器②的名称是 。
(2)从氯化钾溶液中得到氯化钾固体,应选择装置 (填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置 ;从碘水中分离出I2,选择装置 ,该装置的主要仪器名称是 。
(3)实验室中制取的Fe(OH)3胶体中常常含有杂质Cl-离子。可用 的方法除去Fe(OH)3胶体中混有的杂质Cl-离子。
(1)写出下列化学反应的离子方程式
①氢氧化钡溶液和硫酸溶液反应__________________________________
②碳酸钙和足量稀盐酸反应___________________________________
(2)根据下列离子方程式,各写一个符合条件的化学方程式
①Zn+2H+==Zn2++H2↑_______________________________
②HCO3-+ H+==CO2↑+ H2O____________________________________