今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH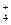 、Ba2+、Cl-、CO
、Ba2+、Cl-、CO 、SO
、SO 。现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,以下推测正确的是
。现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,以下推测正确的是
A.一定不存在Ba2+,NH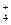 可能存在 可能存在 |
B.CO 一定存在 一定存在 |
| C.Na+一定存在 | D.一定不存在Cl- |
下列有关阿佛加德罗常数(NA)的说法错误的是()
A.32克O2所含的原子数目为NA
B.0.5molSO2含有的原子数目为1.5NA
C.0.5molSO2含有的分子数目为1.5NA
D.0.5NA个氯气分子(标况下)的体积是11.2L
选择萃取剂将碘水中的碘萃取出来,这种萃 取剂应具备的性质是()
取剂应具备的性质是()
A.不溶于水,且必须不与碘发生化学反应 |
| B.不溶于水,且比水更容易使碘溶解 |
| C.不溶于水,且必须比水密度大 |
D.不溶于水, 且必须比水密度小 且必须比水密度小 |
下列电离方程式,书写正确的是()
A.Al2(SO4)3 =2Al3+ + 3SO42- =2Al3+ + 3SO42- |
B.AlCl3 = Al3+ +3Cl- |
| C.Mg(NO3)2 = Mg+2 +2NO3- | D.KMnO4 =K+ +Mn7+ +4O2- |
检验某溶液中是否含有SO42-离子,常用的方法是
| A.取样,滴加BaCl2溶液,看是否有不溶于水的白色沉淀生成 |
| B.取样,滴加稀盐酸酸化的BaCl2溶液,看是否有不溶于水的白色沉淀生成 |
| C.取样,滴加稀盐酸,无明显现象,再滴加BaCl2溶液,看是否有不溶于水的白色沉淀生成 |
D.取样,滴加稀硫酸,再滴加BaCl2溶液,看是否有不溶于水 的白色沉淀生成 的白色沉淀生成 |
物质的量浓度相同的NaCl 、MgCl2、AlCl3三种溶液,当溶液的体积比为3:2:1时,三种溶液中Cl-的物质的量之比为()
A 1 :1:1 B 1:2:3 C 3:2:1 D 3:4:3
:1:1 B 1:2:3 C 3:2:1 D 3:4:3