五种短周期元素的性质或原子结构信息如下表:
| 元素 |
元素性质或原子结构信息 |
| Q |
原子核外有6种不同运动状态的电子 |
| R |
最外层电子数是次外层电子数的3倍 |
| X |
气态氢化物的水溶液 呈弱碱性 呈弱碱性 |
| Y |
第三周期元素的简单离子中离子半径最小 |
| Z |
单质为银白色固体,在空气中燃烧发出黄色火焰 |
请根据表中信息回答下列问题:
(1)Q原子的电子排布式为___________________________,其同位素有 。
(2)R与Z组成的化合物的化学式是 。
(3)X气态氢化物分子的空间构型为 。X的最高价氧化物对应的水化物其浓溶液与同类物质相比在化学性质上表现的特殊性有 。
(4)Y单质与V2O5反应的化学方程式为 。
(5)在1.01×105Pa、298K时,1.4gQR气体在1.6gR2气体中完全燃烧,生成QR2气体时放出14.15kJ热量,表示QR燃烧的热化学方程式为 。
在11到18号元素中,除稀有气体元素外(填符号或化学式)
①原子半径最小的元素是,原子半径最大的元素是;
②非金属性最强的元素是,金属性最强的元素是;
③最高价氧化物对应水化物碱性最强的是,它对应的氧化物的化学式;
④最高价氧化物对应水化物酸性最强的是,它对应的氢化物的化学式;
⑤气态氢化物中最稳定的是,最不稳定的是。
写出下列物质的电子式:
(1)MgCl2(2) CO2(3)NaOH(4) H2O2
、A、B、C、D、E均为有机化合物,它们之间的关系如图所示(提示:RCH=CHR'在酸性高锰酸钾溶液中反应生成RCOOH和R'COOH,其中R和R' 为烷基)。回答下列问题: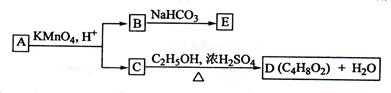
(1)直链化合物A的相对分子质量等于100,A分子中碳、氢元素的总质量分数为0.68,其余为氧元素,则A的分子式为______________
(2)A可以与金属钠作用放出氢气,能使溴的四氯化碳溶液褪色,则A的结构简式是__________。
(3)已知B与NaHCO3溶液完全反应,其物质的量之比为1:2,则在浓硫酸的催化下,B与足量的C2H5OH发生反应的化学方程式 ____________________________,
反应类型为。
(4)D的同分异构体中,能与NaHCO3溶液反应放出CO2的有种,其相应的结构简式是。
以五倍子为原料可制得A,A的结构简式如下图所示,试回答下列问题: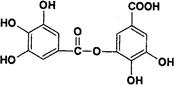
(1)A的分子式为_______________。
(2)有机化合物B在硫酸催化条件下加热发生酯化可得到A。则B的结构简式为______________。
(3)写出A与过量NaOH溶液反应的化学方程式__________________________________。
下列物质的类别与所含官能团都正确的是___________________。