粉煤灰是燃煤电厂排出的工业废渣,其中含莫来石(Al6Si2O13)的质量分数为43.4%,还有含量较多的SiO2(其他成分不含Al和Si)。用粉煤灰和纯碱在高温下烧结,可制取NaAlSiO4(霞石)、Na2SiO3和NaAlO2,有关化学方程式为:
Al6Si2O13 + 3Na2CO3 → 2NaAlSiO4+ 4NaAlO2 + 3CO2↑ ①
Al6Si2O13 + 5Na2CO3→ 2Na2SiO3 + 6NaAlO2 + 5CO2↑ ②
SiO2 + Na2CO3→ Na2SiO3 + CO2↑ ③
(1)粉煤灰中铝的质量分数为 % 。
(2)用1 mol Al6Si2O13 和 4 mol SiO2制得5mol NaAlO2、1mol NaAlSiO4,还应制得Na2SiO3____________mol,共消耗Na2CO3 mol(得到的固体中无SiO2)。
(3)若粉煤灰中 Al6Si2O13 与 SiO2的物质的量之比为1:2,则1kg粉煤灰与6mol Na2CO3反应(反应物全部都参与反应),可制得NaAlO2_________________mol。
(4)若用100 mol Al6Si2O13同时生产NaAlSiO4和NaAlO2,且n(NaAlSiO4):n(NaAlO2) = x,消耗Na2CO3 y mol,试确定y与x的关系式。
如右图所示,已知A元素的最低化合价为-3,它的最高价氧化物含氧56.34%,原子核内中子数比质子数多一个。试完成下列问题:
(1)写出它们的元素符号:
A_________,B_________,C_________,D_________,E_________。
(2)它们的气态氢化物稳定性最弱的是_________。
(3)A、B、C三元素最高价氧化物对应水化物的酸性由强到弱的顺序是_________。
现有A、B、C、D四种元素,A、B元素的原子各有两个电子层,C、D各有三个电子层;A与B能化合成无色、无味的气体AB2;1 mol C单质与0.5 mol D单质能形成离子化合物C2D;B和D同主族,B的离子和C的离子核外电子数相等。试推断这四种元素的名称。
某同学在画某种元素的一种单核微粒的原子结构示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示作出自己的判断。
(1)该微粒是中性微粒,这种微粒的符号是__________。
(2)该微粒的盐溶液能使溴水褪色,并出现浑浊,这种微粒的符号是__________。
(3)该微粒的氧化性很弱,得到1个电子后变为原子,原子的还原性很强,这种微粒的符号是__________。
(4)该微粒的还原性很弱,失去1个电子后变为原子,原子的氧化性很强,这种微粒的符号是__________。


(1)上表中的实线是元素周期表部分边界,请在表中用实线补全元素周期表边界。
(2)元素甲是第三周期ⅥA族元素,请在右边方框中按氦元素的式样,写出元素甲的原子序数、元素符号、元素名称、相对原子质量。
(3)元素周期表体现了元素周期律,元素周期律的本质是原子核外电子排布的____________,请写出元素在元素周期表中的位置与元素原子结构的关系:__________________________。
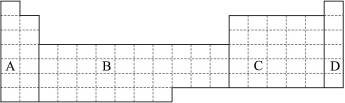
(1)在上面元素周期表中全部是金属元素的区域为____________。
a.A b.B c.C d.D
(2)有人认为形成化合物最多的元素不是ⅣA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是____________。
(3)现在甲、乙两种短周期元素,在室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲、乙两元素比较,金属性较强的是____________(填名称),可以验证该结构的实验是____________。
a.将在空气中放置已久的这两种元素的块状单质分别放入热水中
b.将这两种元素的单质粉末分别与同浓度的盐酸反应
c.将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
d.比较这两种元素的气态氢化物的稳定性