用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A.100mL 1mol/L FeCl3溶液中含阳离子数为0.1NA |
| B.78 g Na2O2中所含阴离子数为1NA |
| C.常温常压下,22.4LCH4气体与足量Cl2反应可生成NA个CH3Cl分子 |
| D.80mL 10mol/L浓盐酸与足量MnO2反应,转移电子数为0.4NA |
如图所示装置,电流表G发生偏转,同时X极逐渐变粗,Y极逐渐变细,Z是电解质溶液,则X、Y、Z应是下列各组中的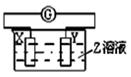
| A.X是Zn,Y是Cu,Z为稀H2SO4 |
| B.X是Cu,Y是Zn,Z为稀H2SO4 |
| C.X是Fe,Y是Ag,Z为稀AgNO3溶液 |
| D.X是Ag,Y是Fe,Z为稀AgNO3溶液 |
下列说法正确的是
| A.冰熔化时,分子中H—O键发生断裂 |
| B.HI比HF易分解,是因为HI分子间不存在氢键 |
| C.CO2与SiO2都属于分子晶体 |
| D.熔沸点由高到低的顺序是:金刚石>NaCl>Na |
苹果醋是一种由苹果发酵而成的食品。苹果酸( )是这种饮料的主要酸性物质。下列有关苹果酸性质的说法中,不正确的是
)是这种饮料的主要酸性物质。下列有关苹果酸性质的说法中,不正确的是
| A.可以与NaHCO3溶液反应产生CO2 |
| B.可以与乙醇发生酯化反应 |
| C.1mol的苹果酸最多能与2mol金属钠反应 |
D.苹果酸与  互为同分异构体 互为同分异构体 |
下列有机反应中,不属于取代反应的是
A.CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O CH3COOCH2CH3+H2O |
B.2CH3CH2OH  CH3CH2OCH2CH3+H2O CH3CH2OCH2CH3+H2O |
C.CH3CH2OH  CH2=CH2↑+H2O CH2=CH2↑+H2O |
D. +Br2 +Br2 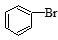 +HBr +HBr |
下列关于有机物的性质或应用说法不正确的是
| A.用饱和的CuSO4溶液使蛋清液发生盐析,进而分离、提纯蛋白质 |
| B.淀粉和纤维素的组成都可用(C6H10O5)n表示,它们都可转化为葡萄糖 |
| C.煤通过干馏可得到焦炭、煤焦油、焦炉气、粗氨水等 |
| D.油脂皂化反应的产物是高级脂肪酸钠和甘油 |