有机物A(C6H8O4)为食品包装纸的常用防腐剂。A可以使溴水褪色。A难溶于水,但在酸性条件下可发生水解反应,得到B(C4H4O4)和甲醇。通常状况下B为无色晶体,能与氢氧化钠溶液发生反应。
(1)A可以发生的反应有 (选填序号)。
①加成反应 ②酯化反应 ③加聚反应 ④氧化反应
(2)B分子所含官能团的名称是 、
(3)B分子中没有支链,其结构简式是  与B具有相同官能团的同分异构体的结构简式是 。
与B具有相同官能团的同分异构体的结构简式是 。
(4)由B制取A的化学方程式是 。
(5)天门冬氨酸(C4H7NO4)是组成人体蛋白质的氨基酸之一,可由B通过以下反应制取: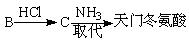
天门冬氨酸的结构简式是 。
甲元素的原子序数是9,乙是元素周期表第三周期中金属性最强的元素,丙元素原子核外有三个电子层,最外层电子层上有6个电子,丁元素比丙多一个质子,由此推断:
(1)甲元素在周期表中位于第二周期的_________族
(2)甲元素的气态氢化物的稳定性比HCl的_________(填“强”或“弱”)
(3)乙元素单质在空气中燃烧,生成一种淡黄色的固体的名称是_________ ,指出它所含的化学键的类型_______________________。
(4)乙元素原子半径比丙元素原子_________(填大或小)
(5)丙元素最高价氧化物的水化物的分子式是_________,它的酸性比磷酸的_________(填“强”或“弱”)
(6)另有A,B,C三种短周期元素,A和B同周期,A和C同主族,三者的原子序数之和为41,三者的最外层电子总数为19,则推断出的元素依次为A________B________C________.(填元素符号)
碳族元素包括
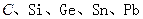 。
。
(1)碳纳米管有单层或多层石墨层卷曲而成,其结构类似于石墨晶体,每个碳原子通过sp2杂化与周围碳原子成键,多层碳纳米管的层与层之间靠 结合在一起。
(2)干冰和晶体碘晶体结构相似,其晶胞平均含个分子,一个分子周围有个紧邻的分子。
(3)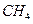 中共用电子对偏向
中共用电子对偏向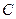 ,
,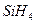 中共用电子对偏向
中共用电子对偏向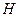 ,则
,则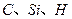 的电负性由大到小的顺序为 。
的电负性由大到小的顺序为 。
(4)用价层电子对互斥理论推断 分子中
分子中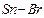 的键角
的键角 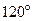 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(5)铅、钡、氧形成的某化合物的晶胞结构是: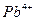 处于立方晶胞顶点,
处于立方晶胞顶点,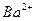 处于晶胞中心,
处于晶胞中心,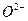 处于晶胞棱边中心,该化合物化学式为 ,每个
处于晶胞棱边中心,该化合物化学式为 ,每个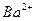 与 个
与 个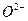 配位。
配位。
(6)金刚石的晶胞平均含个碳原子;单质Au的堆积模型名称为。
(6分)已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系: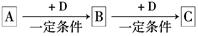
(1)若A能使湿润的红色石蕊试纸变蓝;C为红棕色气体。则A转化为B反应的化学方程式为。
(2)若D是具有氧化性的单质,A元素属于短周期主族金属元素,则C 的电子式为。
的电子式为。
(3)若D是金属,C溶液在贮存时应加入少量D,其理由是(用必要的文字和离子方程式说明)。
(4)若D是一种常见的温室气体;A是一种强电解质且在水溶液中电离出的阴、阳离子均含有10个电子。则B转化为C的离子方程式为。
(5)若D为氯碱工业的主要产品,B具有两性,则C溶液中除氢氧根外还存在的阴离子的化学式为。
(6)若A、B、C均为氧化物,D是一种黑色固态非金属单质,则B分子的结构式为。
某温度下,容积同为2L的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下
(已知某温度下2HI(g)  H2 (g)+I2 (g)
H2 (g)+I2 (g) 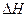 =" +A" kJ·mol
=" +A" kJ·mol K=4.0)
K=4.0)
| 容器 |
甲 |
乙 |
丙 |
| 反应物投入量 |
2 mol HI |
1 mol H2 + 1 1mol I2 |
2 mol HI + 1 mol H2+ 1 mol I2 |
HI的浓度(mol·L ) ) |
c1 |
c2 |
c3 |
| 反应的能量变化 |
放出akJ |
吸收bkJ |
吸收ckJ |
| 体系压强(Pa) |
p1 |
p2 |
p3 |
| 反应物转化率 |
 |
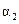 |
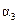 |
(1)根据上表回答问题
①c1、c3的关系式为
②a、b的关系式为
③p2、p3的关系式为
④ 与
与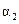 的关系式为
的关系式为
(2)甲容器中:该反应的 平衡常数表达式为。
平衡常数表达式为。
(3)乙容器中:反应在开始2分钟后达平衡状态,则该反应在这2分钟的平均反应速率为mol·L ·min
·min (用含有c2的代数式表示)
(用含有c2的代数式表示)
(4)丙容器中:反应开始时进行的方向是(填“向 左”、“向右”或“不动”)
左”、“向右”或“不动”)
(5)乙容器中:当反应达到平衡状态后,向容器中再充入1 mol H2,则1分钟后,正反应速率与原平衡时相比(填“增大”、“不变”或“减小”)
(8分)
(1)表示含有20个中子的氯原子的符号为
(2)写出4核10电子分子的电子式
(3)已知一氧化碳的燃烧热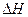 为—283kJ/mol,写出表示一氧化碳燃烧热的热化学方程式
为—283kJ/mol,写出表示一氧化碳燃烧热的热化学方程式
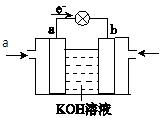
(4)CH3OH与 O2的反应可将化学能转化为电能,其工作原理如图所示,a极的电极反应式是。
O2的反应可将化学能转化为电能,其工作原理如图所示,a极的电极反应式是。