下列说法中不正确的是 ( )
| A.将纯水加热至较高温度,水的离子积变大,pH变小,呈中性 |
| B.氨水和盐酸混合后溶液呈酸性,溶液中离子浓度大小关系一定存在:c(NH4+)>c(H+) |
| C.相同温度下,pH=2的醋酸溶液与pH=2的盐酸中c(H+)之比为1:l |
| D.向盛有少量Mg(OH)2沉淀的试管中加入NH4Cl浓溶液,振荡,沉淀会逐渐溶解 |
已知:X、Y、Z、W为短周期元素,原子半径X:99pm Y: 154pm Z:125pm W: 117pm,X、Y、W位置如图所示(副族省略),X、Y、Z的最高价氧化物对应的水化物相互能反应,下列说法正确的是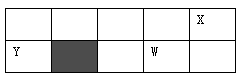
| A.元素Z处于周期表的阴影位置 |
| B.非金属性:X>W |
| C.X与W形成化合物熔点很高,为离子化合物 |
| D.Y、W的最高价氧化物对应的水化物能反应 |
下列有关实验操作、现象和解释或结论都正确的是
| 选项 |
实验操作 |
现象 |
解释或结论 |
| A |
过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 |
溶液呈红色 |
稀HNO3将Fe氧化为Fe3+ |
| B |
AgCl沉淀中滴入稀KI溶液 |
有黄色沉淀出现 |
AgI比AgCl更难溶 |
| C |
Al箔插入稀HNO3中 |
无现象 |
Al箔表面被HNO3氧化,形成致密的氧化膜 |
| D |
用玻璃棒蘸取浓氨水点到红色石蕊试纸上 |
试纸变蓝色 |
浓氨水呈碱性 |
同主族常见的三种元素X、Y、Z,它们最高价氧化物对应水化物的酸性强弱顺序为:HXO4<HYO4<HZO4,下列判断不正确的是
| A.Y 单质可以在海水中提取 |
| B.单质氧化性: Y>Z |
| C.气态氢化物稳定性:HX<HZ |
| D.离子半径: X->Y- |
下列各项叙述Ⅰ,Ⅱ都正确且二者的原理最相似的是
| 叙述Ⅰ |
叙述Ⅱ |
|
| A |
FeS难溶于水,却溶于稀硝酸 |
CaCO3难溶于稀硫酸,却溶于醋酸 |
| B |
浓硝酸要密封保存阴凉处 |
漂白粉要密封保存在阴凉处 |
| C |
盐酸与铁反应生成氯化亚铁 |
少量氯气与铁反应生成氯化亚铁 |
| D |
碳酸钠溶液显弱碱性 |
氯化铵溶液显弱酸性 |
下列有关化学实验的叙述正确的是
| A.用待测液润洗滴定用的锥形瓶 |
| B.配制FeCl3溶液时,向溶液中加入少量Fe和稀盐酸 |
| C.用稀硝酸洗涤做过银镜反应的试管 |
| D.液溴保存时液面覆盖一层水,装在带橡胶塞的试剂瓶中 |