1mol某烃A和1 mol苯完全燃烧,烃A比苯多消耗1mol O2,若A分子结构中无支链或侧链,则:(1)若A为环状化合物,它能与等物质的量的Br2发生加成反应,则A的结构简式为 ;
(2)若A为链状烯烃,1mol A最多可和2mol Br2发生加成反应且A与等物质的量的Br2加成后的可能产物只有2种,则A的结构简式为 。
某芳香烃X是一种重要的有机化工原料,质谱法测定其相对分子质量为92.现以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去),其中A是一氯代物,F的分子式为C7H7NO2,Y是一种功能高分子材料。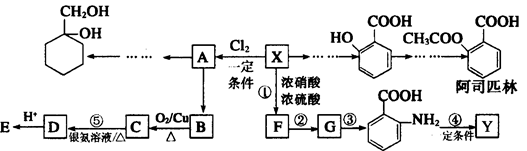
已知:
请根据所学知识与本题所给信息回答下列问题:
(1)X的化学式是_____________,其核磁共振氢谱图有____________个吸收峰;
(2)反应⑤的化学方程式是______________________________;
(3)阿司匹林分子中含有的官能团的名称是______________;1mol阿司匹林与足量NaOH溶液反应最多消耗NaOH的物质的量为_____________________。
(4)Y的结构简式为___________________________________。
(5) 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有 _________种;
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有 _________种;
(6)以下是由A和其它物质合成 的流程图,
的流程图,
甲→乙反应的化学方程式为_______________________________________________。
有机物A的分子式为C9H10O2,A在光照条件下生成一溴代物B,B分子的核磁共振氢谱中有4组峰,峰面积比为2:2:2:3,B可发生如下转化关系(无机产物略):
已知:①K与氯化铁溶液发生显色反应,且环上的一元取代物只有两种结构;
②当羟基与双键碳原子相连时,会发生如下转化:RCH=CHOH→RCH2CHO;
请回答下列问题:
(1)B中含氧官能团的名称是,反应①~⑤中属于取代反应的是。
(2)写出结构简式:G,E。
(3)写出下列反应的化学方程式:
反应①:,
反应③:。
(4)同时符合下列要求的K的同分异构体有种;
写出其中任意一种同分异构体的结构简式:。
Ⅰ.苯环上的一元取代物只有两种结构
Ⅱ.能发生银镜反应
Ⅲ.与氯化铁溶液发生显色反应
(1)有机物A由C、H、O三种元素组成,其蒸气密度是同温同压下氢气密度的23倍,核磁共振氢谱显示其分子中有3种氢原子且个数比为3:2:1 。有机物A的分子式为。
(2)芳香化合物B的分子式为C7H8O,B能与金属钠反应,不与强碱反应。B中所含官能团的名称;B的同分异构体中能与FeCl3溶液发生显色反应的物质有多种,请任写一种结构简式。
(3)用A和B为原料完成以下转化:
已知:①两个醛分子间能发生如下反应: (﹣R、﹣R’表示氢原子或烃基)
(﹣R、﹣R’表示氢原子或烃基)
③1mol H分别与足量的金属钠、碳酸氢钠溶液反应时,均生成22.4L气体(标准状况)。
回答下列问题:
① C + D E的反应类型为;E
E的反应类型为;E F反应的反应类型为____________。
F反应的反应类型为____________。
②F的结构简式为:。
③写出下列转化的化学方程式:
B D 。
D 。
D K。
K。
H I。
I。
④满足下列条件的F有多种同分异构体,
Ⅰ. 该物质和FeCl3溶液能发生显色反应;
Ⅱ.该物质能使Br2的CC14溶液褪色;
Ⅲ.该物质分子中只有一个甲基。
写出其中苯环上取代基数目不同的任意两种同分异构体的结构简式。
Ⅰ.请选出下列各题中符合题意的选项:
(1)下列不可能存在的有机物是
A.2—甲基丙烷 B.2,3—二氯—2,2—二甲基戊烷
C.3—溴—3—乙基戊烷 D.2,2,3,3—四甲基丁烷
(2)能在KOH的醇溶液中发生消去反应的是
(3)某有机物既能发生氧化反应,又能发生还原反应,且氧化产物和还原产物能发生酯化反应,所生成的酯也能发生银镜反应。则该有机物的结构简式是
A.CH3OH B.HCHO
C.HCOOH D.HCOOCH3
Ⅱ.有机物A的结构简式为: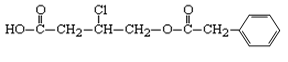
据此回答下列问题:
(1)A的分子式为__________。
(2)A在NaOH水溶液中加热,经酸化得到有机物B和D,D是芳香族化合物。当有1 mol A发生反应时,最多消耗mol NaOH。
(3)B在一定条件下发生酯化反应可生成某五元环酯,该五元环酯的结构简式为。
(4)写出苯环上只有一个取代基且属于酯类的D的所有同分异构体的结构简式:。
(1)有下列六组物质:属于同系物的是,属于同分异构体是,属于同种物质的是。(填序号) 
(2)A.某烃与2倍的氢气加成后得到2,2-二甲基丁烷,按系统命名法,该烃的名称是。
B.下图是某有机物结构简式, 按系统命名法,该有机物的命名正确的是。