一种将CO2变为燃料或有机化学品的构想分成3个步骤:
①利用浓碳酸钾溶液吸收空气中的CO2;
②将第①步吸收液电解产生H2和O2,同时分离出CO2;
③将第②步产生的H2和CO2在一定条件下转化成CH4和H2O2。
已知:H2(g)+ O2(g)=H2O(l) △H1=—285.8kJ/mol
O2(g)=H2O(l) △H1=—285.8kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H2=—889.6kJ/mol
H2O(l)=H2O(g) △H3=+44.0kJ/mol
(1)第③步反应的热化学方程式为 。W ww.k s5u.co m
|
(2)若在第②步电解吸收液时产生11.2LO2(标准状况下),则第③步中最多可制得 L甲烷(标准状况下)
(3)为探究在密闭容器中进行第③步反应的最佳投料比,某现有金属单质A、B、C、I和气体甲、乙、丙及物质D、E、F、G、H。其中B是地壳中含量最多的金属。它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。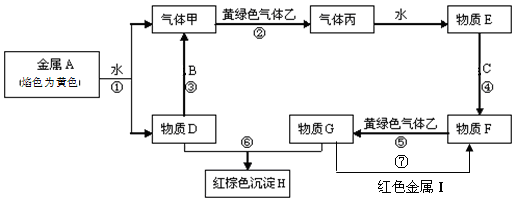
请根据以上信息回答下列问题:
(1)写出下列物质的化学式: CH
(2)写出反应①的离子方程式:。
写出反应⑦的离子方程式:。
(3)气体乙与SO2气体都具有漂白性,将等体积的气体乙和SO2通入到水中,得到的溶液是否具有漂白性?(填“是”或“否”)。反应的化学方程式:。
按要求填空:
(1)除去NaHCO3溶液中的少量Na2CO3,方法是:;离子方程式为:。
(2)呼吸面具中所用的药品是;反应的化学方程式为:。
(3)由铝盐制取氢氧化铝,所用的试剂为:;离子方程式为:。
(4)白色的Fe(OH)2在空气中发生的颜色变化为。
(5)写出硅酸钠溶液在空气中变质的化学方程式:。
(6)写出用熟石灰吸收氯气制漂白粉的化学方程式:。
(7)将CaMg3Si4O12改写为氧化物的形式:。
(12分)现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。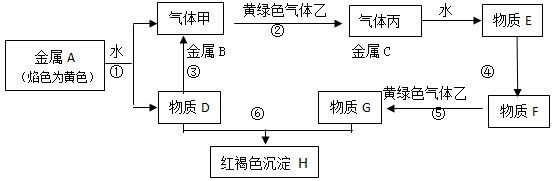
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:
A; B; C;F; H;乙。
(2)写出下列反应离子方程式:
反应①
反应⑤
反应⑥
(10分)
(1)5 mol H2O的质量为______,其中含有__________个水分子,氢原子的物质的量为______。
(2)质量相同的H2、NH3、SO2、O3四种气体中,含有分子数目最少的是_________,在相同温度和相同压强条件下,体积最大的是_______。
(6分)用双线桥法标出下列反应中电子转移的方向和数目,并回答下列相关问题:
2KMnO4 + 16HCl(浓) =" 2KCl" + 5Cl2↑ + 2MnCl2 + 8H2O
(1)该反应中,氧化剂是,元素被氧化;
(2)若反应消耗1 mol氧化剂,则被氧化的还原剂的物质的量是mol;
(3)该反应的离子方程式是。