(1)爱迪生蓄电池在放电时的总反应方程式为:Fe+NiO2+2H2O=Fe(OH)2+Ni(OH)2
该电池的电解质溶液应为: (选“酸性”或“碱性”)溶液
正极反应式为: 负极反应式为:
(2)下面是中学化学实验中常见的几种定量仪器:
a、量筒 b、容量瓶 c、托盘天平 d、温度计
①其中标示出仪器使用温度的是_____________(填写编号);
②使用前要检查仪器是否漏液的是____________________(填写编号);
③称取10.5g固体样品(1g以下使用游码)时,将样品放在了天平的右盘,则所称样品的实际质量为_______________g。
某化学反应2A  B+D在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为______________mol/(L·min)。
(2)在实验2,A的初始浓度C2=________mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是 。
(3)实验3的反应速率为V3,实验1的反应速率为V1,则V3 V1,且C3 1.0mol/L(填>、=、<)。
(4)比较实验4和实验1,可推测该反应是_________反应(选填吸热、放热)。理由_____________。
甲醇(CH3OH)是一种重要的化工原料,广泛应用于化工生产,也可以直接用作燃料.已知:
CH3OH(l)+O2(g)===CO(g)+2H2O(g)ΔH1=-443.64 kJ/mol
2CO(g)+O2(g)===2CO2(g)ΔH2=-566.0 kJ/mol
(1)试写出CH3OH(l)在氧气中完全燃烧生成CO2和H2O(g)的热化学方程式_________________。
(2)科研人员新近开发出一种由强碱作电解质溶液的新型甲醇手机电池,可使手机连续使用一个月才充一次电,据此回答:甲醇在________极反应。
(3)利用电池可实现电能向化学能的转化。某同学设计了一种用电解法制取Fe(OH)2的实验装置(如图),通电后,溶液中产生大量的白色沉淀,且较长时间不变色.下列说法中不正确的是________(填序号)。
A.电源中的a一定为正极,b一定为负极
B.可以用NaCl溶液作为电解质溶液
C.A、B两端都必须用铁作电极
D.阴极发生的反应是2H++2e-===H2↑
将煤转化为水煤气的主要化学反应为C(s)+H2O(g)===CO(g)+H2(g); C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
C(s)+O2(g)===CO2(g)ΔH=-393.5 kJ/mol
H2(g)+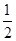 O2(g)===H2O(g)ΔH=-242.0 kJ/mol
O2(g)===H2O(g)ΔH=-242.0 kJ/mol
CO(g)+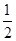 O2(g)===CO2(g)ΔH=-283.0 kJ/mol
O2(g)===CO2(g)ΔH=-283.0 kJ/mol
请回答下列问题:
(1)根据以上数据,写出C(s)与水蒸气反应的热化学方程式____________________。
(2)比较反应热数据可知,1 mol CO(g)和1 mol H2(g)完全燃烧放出的热量之和比 1mol C(s)完全燃烧放出的热量多.甲同学据此认为“煤转化为水煤气可以使煤燃烧放出更多的热量”;乙同学根据盖斯定律作出如下列循环图:
并据此认为“煤转化为水煤气再燃烧放出的热量与煤直接燃烧放出的热量相等”。
请分析:甲、乙两同学观点正确的是________(填“甲”或“乙”),判断的依据是________。
(3)将煤转化为水煤气作为燃料和煤直接燃烧相比有很多优点,请列举其中的两个优点:
____________________、____________________。
(4)水煤气不仅是优良的气体燃料,也是重要的有机化工原料.CO和H2在一定条件下可以合成: ①甲醇(CH4O) ②甲醛(CH2O) ③甲酸(CH2O2) ④乙酸(C2H4O2).试分析当CO和H2按1:1的体积比混合反应,合成上述________(填序号)物质时,可以满足“绿色化学”的要求,完全利用原料中的原子,实现零排放。
在一个小烧杯里,加入 20 g Ba(OH)2·8H2O粉末,将小烧杯放在事先已滴有4~5滴水的玻璃片上.然后加入10g NH4Cl晶体,并用玻璃棒迅速搅拌.如下图所示。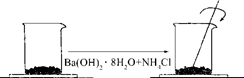
回答下列问题:
(1)实验中玻璃棒的作用是______________________________;
(2)反应方程式是____________________,该反应属于________(填反应类型);
(3)实验中观察到现象有_____________;反应混合物呈糊状的原因是____________________;
(4)通过________现象,说明该反应为________热反应,这是由于反应物的总能量________生成物的总能量。
合成具有良好生物降解性的有机高分子材料是有机化学研究的重要课题之一。聚醋酸乙烯酯(PVAc)水解生成的聚乙烯醇(PVA),具有良好生物降解性,常用于生产安全玻璃夹层材料PVB。有关合成路线如下图(部分反应条件和产物略去)。

请回答:
(1)A为饱和一元醇,其氧的质量分数约为34.8%,A的化学名称为_____________,PVA的结构简式为_________________。
(2)C中官能团的名称是____________,C的名称_________________,A~F中核磁共振氢谱出峰最多的是________________(填化合物代号)。
(3)反应①包含的反应类型是_________________;反应④的化学方程式为_________。
(4)PVAc是由F加聚而成,与F具有相同官能团的同分异构体还有_______种;写出其中一种的结构简式:________________。