在一定条件下,将3mol A和1mol B两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)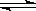 xC(g)+2D(g)。2min末该反应达到平衡,生成0.8mol D,并测得C的浓度为0.2mol·L-1。下列判断错误的是
xC(g)+2D(g)。2min末该反应达到平衡,生成0.8mol D,并测得C的浓度为0.2mol·L-1。下列判断错误的是
| A.x=1 |
| B.2min内A的反应速率为0.3 mol·(L·min)-1tesoon |
| C.该反应达到平衡状态时A的物质的量与总物质的量之比为2:5 |
| D.若混合气体的压强不变,则表明该反应已达到平衡状态 |
已知:HCN(aq)与NaOH(aq)反应的ΔH=-12.1 kJ/mol;HCl(aq)与NaOH(aq)反应的ΔH=-55.6 kJ/mol则HCN在水溶液中电离的ΔH等于( )
| A.-67.7 kJ/mol | B.-43.5 kJ/mol |
| C.+43.5 kJ/mol | D.+67.7 kJ/mol |
某反应过程中体系的能量变化如图所示,下列说法错误的是
A.反应过程可表示为 |
| B.E1为反应物的平均能量与过渡态的能量差,称为正反应 的活化能 |
| C.正反应的热效应为ΔH=E1-E2<0,所以正反应为放热反应 |
| D.此图中逆反应的热效应ΔH=E1-E2<0,所以逆反应为放热反应 |
人类将在未来几十年内逐渐由“碳素燃料文明时代”过渡至“太阳能文明时代”(包括风能、生物质能、太阳能的转换),届时人们将适应“低碳经济”和“低碳生活”。下列说法不正确的是
| A.目前研究菠菜蛋白质“发电”不属于“太阳能文明” |
| B.发展太阳能经济有助于减缓温室效应 |
| C.太阳能电池可将太阳能直接转化为电能 |
| D.煤、石油和天然气都属于碳素燃料 |
某同学用NaHCO3和KHCO3组成的混合物进行实验,测得如下数据(盐酸的物质的量浓度相等)。下列分析推理正确的是
| 盐酸 |
50 mL |
50 mL |
50 mL |
| m(混合物) |
9.2 g |
14.2 g |
27.6 g |
| V(CO2)(标准状况) |
2.24 L |
3.36 L |
3.36 L |
A.盐酸的物质的量浓度为3.0 mol/L
B.当混合物质量为9.2 g时,50 mL盐酸恰好完全反应
C.混合物中NaHCO3、KHCO3的物质的量之比为1∶2
D.混合物中NaHCO3的质量分数为45.7 %
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化关系如图所示。下列说法不正确的是
| A.Cl2和苛性钾溶液在不同温度下可能发生不同反应 |
| B.反应中转移电子数为是0.42 NA |
| C.原苛性钾溶液中KOH的物质的量为0.3 mol |
| D.生成物中Cl-的物质的量为0.21 mol |