有机物的结构可用“键线式”简化表示,如:CH3-CH=CH-CH3可表示为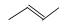 ,有一种有机物X它的键线式如下:
,有一种有机物X它的键线式如下: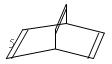
(1)X的分子式为: ;有机物Y是X的同分异构体,且属于芳香族
化合物。则Y的结构简式是 。
(2)Y可以与溴水反应,其生成物的结构简式是 ; Y在一定条件下
还可生成高分子化合物,写出该反应的化学方程式 。
浓硫酸在下列用途和现象中所表现的性质是
| A.沸点高、难挥发 | B.酸性 | C.吸水性 | D.脱水性 E.强氧化性 |

莽草酸是合成治疗禽流感的药物——达菲(Tamiflu)的原料之一。莽草酸是A的一种异构体。A的结构简式如下: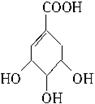 (提示:环丁烷
(提示:环丁烷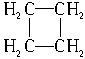 可简写成
可简写成 )
)
(1)A的分子式是_________。
(2)A与溴的四氯化碳溶液反应的化学方程式(有机物用结构简式表示)是_________________________。
(3)A与氢氧化钠溶液反应的化学方程式(有机物用结构简式表示)是___________________________。
(4)1.74 g A与足量碳酸氢钠溶液反应,计算生成二氯化碳的体积(标准状况)。
(5)A在浓硫酸作用下加热可得到B(B的结构简式为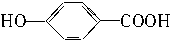 ),其反应类型是_________。
),其反应类型是_________。
(6)B的同分异构体中既含有酚羟基又含有酯基的共有__________种,写出其中一种同分异构体的结构简式___________________。
A和B两种物质的分子式都是C7H8O,它们都能跟金属Na反应放出H2;A不溶于NaOH溶液而B能溶于NaOH溶液,B能使适量浓溴水褪色,并产生白色沉淀,A不能;B的一溴代物有两种结构。则A和B的名称及结构简式为:A_____________,B_____________。
某工业反应混合液中仅可能含有的组分是:乙醚(C4H10O)、乙醇(C2H6O)和水。经分析,液体中各原子的物质的量之比为n(C)∶n(H)∶n(O)=16∶42∶5。
(1)若混合液中只含两种组分,则所有可能的组合是_________________。
(2)若混合液中含有三种组分,在628 g混合液中有1 mol H2O,此时乙醇和乙醚的物质的量各是_______________。
根据下面合成路线完成有关问题: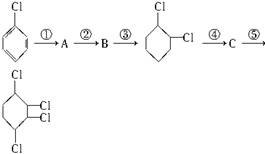
(1)写出A、B、C结构简式:A:____________,B:____________,C:____________。
(2)各步反应类型:①_________,②_________,③_________,④_________,⑤________。
(3)A→B的反应试剂及条件:____________________。