现有A、B两种有机化合物,已知:① B分子可以看成A分子中一个氢原子被氨基取代而得到;②它们的分子中氢元素的质量分数相同,相对分子质量都不超过170,A中碳元素的质量分数为72.00%;③它们都是一取代苯,分子中都不含甲基,都含有一个羧基。
请按要求填空:
(1)A、B的分子中氢元素的质量分数都是 ;B的分子式为 。
(2)A的结构简式是 ;
(3)C与A互为同分异构体,分子中也没有甲基,但苯环上有两个处于对位的取代基,能发生银镜反应,也能在一定条件下发生消去反应,则C与银氨溶液反应的化学方程式是 ;
(4)B有一种同分异构体D是某芳香烃发生硝化反应生成的唯一一种一硝基取代物(硝基连在苯环上),则D的结构简式是 。
电解原理常应用于工业生产
(1)火法炼铜得到的粗铜中含多种杂质(如锌、金、银等),其性能远不能达到电气工业的要求,工业上常使用电解精炼法将粗铜提纯。在电解精炼时,若用硫酸铜溶液作电解液,粗铜接电源 极,电极反应为 ;通电一段时间后,溶液中铜离子浓度将 (增大,不变,减少)。
(2)工业上用电解饱和食盐水的方法可制得烧碱、氯气、氢气。电解时,总离子反应
式为 ;电解时所需的精制食盐水,通常在粗盐水
加入某些试剂(现提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液来、BaCl2
溶液、Ba(NO3)2溶液、盐酸)除去其中的Ca2+、Mg2+、Fe3+、SO42-杂质离子,选出试剂,
按滴加的先后顺序为 (填所加试剂的化学式)。
(3)为了避免产物相混合发生副反应,工业上采用离子交换膜法电解食盐水。下图为阳离
子交换膜法电解饱和食盐水原理示意图。
|
下列说法中正确的是
| A.从E口逸出的气体是H2 |
| B.从B中加入含少量NaOH的水溶液以增强导电性 |
| C.标准状况下每生成22.4L Cl2,便产生2mol NaOH |
| D.向电解后的阴极溶液中加适量盐酸,可以 |
恢复到电解前的物质的浓度
如右图所示,常温下电解5 min后,铜电极质量增加2.16g。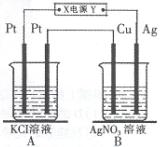
试回答:
(1)电源电极X名称为(填“正极”或“负极”),B中铜电极的名称。
(2)电解池B中阳极的电极反应式是。
(3)若A中KCl溶液的体积是200mL,电解后溶液的
PH=(忽略电解前后溶液体积的变化)。
若要使电解后的溶液恢复到与电解前完全相同,应
加入。
电解原理在化学工业中有广泛应用。右图表示一个电解池,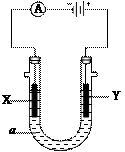
装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。
请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同
时在两边各滴入几滴酚酞试液,则
①Y电极上的电极反应式为,
检验该电极反应产物的方法是。
②电解池中X极上的电极反应式为。
在X极附近观察到的现象是。
③电解一段时间后,若收集到H2为2L,则同样条件下收集的Cl22L(填“>”“<”“=”),
原因是。
(2)如果在铁件的表面镀铜防止铁被腐蚀,电解液a选用CuSO4溶液,请回答:
①X电极对应的金属是______(写元素名称),其电极反应式。
②若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二
者质量差为5.12 g,则电镀时电路中通过的电子为________________mol。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因
。
肼(N2H4)又称联氨,是一种可燃性液体,用作火箭燃料。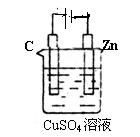
(1)32.0g该液态化合物在氧气中完全燃烧生成氮气放出热量624kJ(25°C,101kPa),则肼完全燃烧的热化学方程式 。
(2)肼——空气燃料电池是一种无污染的清洁的碱性燃料电池,电解质溶液是20%—30%的KOH溶液。该电池放电时,作负极的燃料是 (填化学式);正极的电极反应式是 。
(3)右图是一个电化学过程示意图。
①锌片上发生的电极反应是________________________。
②假设使用肼一空气燃烧电池作为本过程中的电源,锌片的质量
变化是128g,则肼一空气燃料电池理论上消耗标准状况下的空气_____L
(假设空气中氧气体积含量为20%)
X、Y、Z均为短周期非金属元素的单质。在一定条件下有如下反应:Y+X→A(气体),Y+Z→B(气体)。请针对以下两种不同情况回答:
(1)若常温下X、Y、Z均为气体,A和B化合时有白烟产生,德国化学家哈伯因为研究A的工业合成曾两度获得诺贝尔奖,则:
①有人说,哈伯解决了全世界人的吃饭问题,请你说说对这句话的理解。
②A与氧气反应生成C和D,是化工生产上的重要反应,写出该反应的化学方程式,C是大气污染物,说出一种C造成污染的现象,
③将C与A混合,在一定条件下可转化为无毒的X和D,该反应中氧化产物与还原产物的质量之比为。
(2)若常温下Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,则:
①B的化学式是;
②向苛性钠溶液中通入过量的A,所发生反应的离子方程式是;
③将Y与(1)中Z单质的水溶液充分反应可生成两种强酸,该反应的化学方程式是。