A、B、C、D 4种元素,其中A、B、C为短周期元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C。
(1)B元素的名称 ;B在周期表中的位置第 周期,第 族;
(2)A、B形成的化合物的电子式 ;
(3)C的元素符号 ,C的最高价氧化物的化学式 ;
(4)D的最高价氧化物对应的水化物的化学式 。
二氧化钛是一种重要的工业原料。
(1)实验室可通过以下方法制得: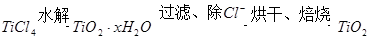
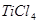 水解生成
水解生成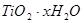 的化学方程式是_________;检验
的化学方程式是_________;检验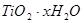 中
中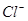 是否被除净的方法是_________。
是否被除净的方法是_________。
(2)工业上可用含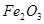 的钛铁矿(主要成分为
的钛铁矿(主要成分为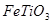 ,其中
,其中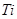 化合价为+4价)制取,其主要流程如下:
化合价为+4价)制取,其主要流程如下: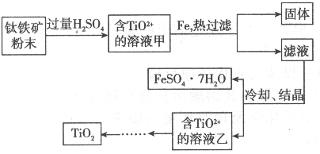
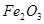 与硫酸反应的离子方程式是________________;向甲溶液中加入铁的目的是________________。
与硫酸反应的离子方程式是________________;向甲溶液中加入铁的目的是________________。
(3)二氧化钛可用于制取金属钛,其步骤如下: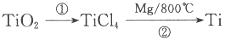
反应②的方程式是________________,该反应需要在 的气氛中进行,原因是________________。
的气氛中进行,原因是________________。
高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂。
(1)Na2FeO4中铁元素的化合价是价,Na2FeO4具有较强的(填“氧化性”或“还原性”)。
(2)用Na2FeO4给水消毒、杀菌时得到的Fe3+可以净水,Fe3+净水原因是(用离子方程式表示)。
(3)工业上可用FeCl3、NaOH 、NaClO三种物质在一定条件下反应制得Na2FeO4,完成下列化学方程式:2FeCl3 + 10NaOH + 3NaClO = 2+ 5+ 9。
(4)工业上还可用电解浓NaOH溶液的方法制Na2FeO4 。
① 若电解所需的浓NaOH溶液为16 mol/L,则在实验室配制500 mL该浓度的溶液需NaOHg,配制过程所需玻璃仪器是。
② 电解浓NaOH溶液制备Na2FeO4,其工作原理如下图所示: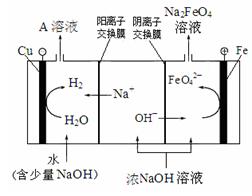
阳极的电极反应式是;可循环使用的物质是,理由是。
电解铝厂的实验室为测定铝土矿(主要成分是Al2O3,杂质是Fe2O3 、SiO2)样品中Al2O3的质量分数,操作如下:
Ⅰ.将铝土矿样品粉碎后加入足量稀H2SO4溶液,充分反应后过滤,得滤液a
Ⅱ.向滤液a中加入足量NaOH溶液,充分反应后过滤,得滤液b
Ⅲ.向滤液b中通入足量CO2,充分反应后过滤、洗涤,得Al(OH)3沉淀
Ⅳ.……
(1)滤液a中阳离子有(写离子符号)。
(2)操作Ⅱ中反应的离子方程式是。
(3)操作Ⅳ是。
(4)要测定铝土矿样品中Al2O3的质量分数,所需数据是(质量数据用x、y…表示,单位是g);铝土矿样品中Al2O3质量分数表达式是(用含x、y…的式子表示)。
甲醇汽油是一种新能源清洁燃料,可以作为汽油的替代物。工业上可用CO和H2制取甲醇,化学方程式为:CO(g)+2H2(g) CH3OH(g) △H="a" kJ/mol
CH3OH(g) △H="a" kJ/mol
为研究平衡时CO的转化率与反应物投料比( )及温度的关系,研究小组在10 L的密闭容器中进行模拟反应,并绘出下图:
)及温度的关系,研究小组在10 L的密闭容器中进行模拟反应,并绘出下图:
(1)反应热a 0 (填“>”或“<”),判断依据是。
(2)若其它条件相同,Ⅰ、Ⅱ曲线分别表示投料比不同时的反应过程。
①投料比:ⅠⅡ (填“>”或“<”)。
②若Ⅱ反应的n(CO)起始 ="10" mol、投料比为0.5,
A点的平衡常数KA=,
B点的平衡常数KBKA (填“>”或“<”或“=”)。
(3)为提高CO转化率可采取的措施是(至少答出两条)。
制作软质隐形眼镜高分子材料(M)和聚酯PET的合成路线如下:
已知酯与醇可发生如下酯交换反应:
(R、R′、R″代表有机基团)
(1)A的相对分子质量是28,A、B分子中含有的官能团分别是。
(2)B的名称是。
(3)反应I的反应类型是_______(选填字母)。
a.加聚反应b.缩聚反应
(4)有关B、C、D的说法正确的是。
a.1mol B最多可以和1 mol C反应
b.C、D都能使Br2的CCl4溶液褪色
c.D与NaOH溶液共热后可以得到B和C
(5)B→D的化学方程式是。
(6)C有多种同分异构体,其中一种是合成纤维维尼纶的单体,该分子在酸性环境下水解得到两种产物,它们的相对分子质量相差16,该同分异构体的结构简式是。
(7)反应II的化学方程式是。