通过粮食发酵可获得某含氧有机化合物,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%。
(1)的分子式是;
(2)与金属钠反应放出氢气,反应的化学方程式是(有机物用结构简式表达);
(3)与空气中的氧气在铜或银催化下反应生成,的结构简式是;
(4)与高锰酸钾酸性溶液反应可生成。在加热和浓硫酸作用下,与反应可生成一种有香味的物质,若184 和120 反应能生成106 ,计算该反应的产率为。
肉桂醛(C9H8O)是一种常用香精,在食品、医药化工等方面都有应用。肉桂醛与其他有机物具有如下转化关系,其中A为一氯代烃。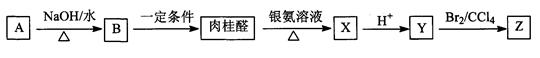
(1)肉桂醛是苯的一取代物,与H2加成的产物中没有支链,肉桂醛结构简式是_______。
(2)反应A→B的化学方程式是_____________________________________________。
(3)Z不能发生的反应类型是(填字母)___________。
a. 取代反应 b. 加聚反应 c. 加成反应 d. 消去反应
(4)Y与乙醇在一定条件下反应的化学方程式是
___________________________________________________________________。
(5)写出符合下列条件的Y的一种同分异构体的结构简式:
___________________________________________________________________。
①属于酯类 ②苯环上只有一个取代基 ③能发生银镜反应。
PtCl2(NH3)2可以形成两种固体,一种为淡黄色,在水中的溶解度小,另一种为黄绿色,在水中的溶解度较大,请回答下列问题:
⑴PtCl2(NH3)2是平面正方形结构,还是四面体结构
⑵请在以下空格内画出这两种固体分子的几何构型图,
淡黄色固体:,黄绿色固体:
⑶淡黄色固体物质是由分子组成,黄绿色固体物质是由分子组成(填“极性分子”或“非极性分子”)
⑷黄绿色固体在水中溶解度比淡黄色固体大,原因是。
有下列分子或离子:(1)BF3(2)H2O(3) NH4+
(4)SO2 (5)HCHO(6)PCl3(7)CO2
粒子构型为直线型的为:粒子的立体构型为V型的为:粒子的立体构型为平面三角形的为:粒子的立体构型为三角锥型的为::粒子的立体构型为正四面体的为。
根据下列五种元素的电离能数据(单位:kJ/mol),回答下面各题。
| 元素代号 |
I1 |
I2 |
I3 |
I4 |
| Q |
2080 |
4000 |
6100 |
9400 |
| R |
500 |
4600 |
6900 |
9500 |
| S |
740 |
1500 |
7700 |
10500 |
| T |
580 |
1800 |
2700 |
11600 |
| U |
420 |
3100 |
4400 |
5900 |
(1)在周期表中,最可能处于同一族的是()
A.Q和R B.S和T C.T和U D.R和T E.R和U
(2)电解它们的熔融氯化物,阴极放电反应最可能正确的是()
A.Q2++2e-→Q B.R2++2e-→R
C.S3++3e-→S D.T3++3e-→TE.U2++2e-→U
(3)它们的氯化物的化学式,最可能正确的是()
A.QCl2 B.RCl C.SCl3 D.TCl E.UCl4
(4)S元素最可能是()
A.S区元素 B.稀有气体元素 C.p区元素D.准金属E.d区元素
(5)下列元素中,化学性质和物理性质最像Q元素的是()
A.硼(1s22s22p1) B.铍(1s22s2) C.锂(1s22s1)D.氢(1s1) E.氦(1s2)
氯化溴(BrCl)的化学性质类似于卤素单质,试回答下列问题:
(1)氯化溴的电子式是,它是由键形成的分子。
(2)氯化溴和水反应生成了一种三原子分子,该分子的电子式为。