某研究小组为了探究“铁与水蒸气”能否发生反应及反应的产物,进行了系列实验。
(1)用下图所示实验装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”(石棉绒是耐高温材料,不与水反应)。反应一段时间后,有肥皂泡吹起时,用点燃的火柴靠近肥皂泡,当
时(填实验现象),说明“铁与水蒸气”能够进行反应。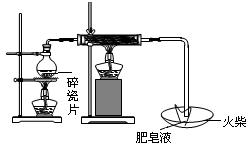
(2)为了研究一定时间内铁粉的转化率,他们设计了如下实验:准确称取一定质量的铁粉进行反应,收集并测量反应后生成的气体体积,计算出铁粉的转化率。
①收集并测量气体体积应选右图中的________装置(填A或B)。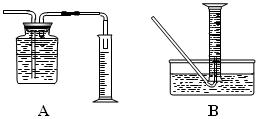
②称取0.24g铁粉与适量石棉绒混合,然后加热至无气体放出。若室温下氢气密度约为0.088g/L,最好选用 规格的量筒(选填字母序号)
A.100mL B.200mL C.500mL D.1000mL
③收集的气体体积为VL,铁粉的转化率为 。
(3)为了证明反应后的固体混合物中含有+3价的Fe,他们计划取出少量混合物于试管中,加入足量的盐酸,溶解、过滤。向滤液中滴加KSCN溶液,观察溶液的颜色。在下表中填写滴加KSCN溶液后可能观察到的现象、结论与解释(可以不填满)。
| |
现象 |
结论与解释 |
| 可能① |
|
|
| 可能② |
|
|
氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:
回答下列问题:
(1)①加碳酸钠溶液并小火加热的操作目的是;
②操作Ⅰ的名称是________,操作Ⅱ的名称是_________;
(2)①流程所发生的反应为FeSO4 + 2NH4HCO3 = FeCO3↓+ (NH4)2SO4 + CO2↑过程中,加入稍过量的NH4HCO3溶液后,且要控制溶液的为6.8~7.2之间。加入稍过量的目的是,溶液的pH不能过低的原因是。
②检验滤液B中含有NH4+的方法是。
(3)有些同学认为KMnO4溶液滴定能进行铁元素含量的测定。
a.称取2.850g绿矾(FeSO4·7H2O)产品,配成250mL溶液;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
①写出酸性KMnO4溶液与FeSO4 溶液反应的离子方程式。
②用KMnO4标准溶液滴定时应选用______滴定管(填“酸式”或“碱式”)。
③计算上述样品中FeSO4·7H2O的质量分数为[已知M(FeSO4·7H2O)="278g/mol]" 。
(16分) Na2S2O3可用作照相的定影剂等。已知Na2S2O3的某些性质如下:
(1)S2O32-能被I2氧化为S4O62-;
(2)酸性条件下S2O32-迅速分解为S和SO2
Ⅰ.市售Na2S2O3中常含有SO42-, 请完成以下方案,检验其中含有的SO42-:
| 实验步骤 |
预期现象或结论 |
| 步骤1:取少量固体样品溶于无氧蒸馏水中 |
固体完全溶解得无色澄清溶液 |
| 步骤2: |
|
| 步骤3: |
Ⅱ.利用K2Cr2O7标准溶液可以定量测定市售硫代硫酸钠试剂的纯度,步骤为:
① 溶液配制:称取1.0gNa2S2O3试样,用新煮沸并冷却的蒸馏水溶解,最终定容至100mL。
② 滴定:取10.00mL0.01mol·L-1K2Cr2O7标准溶液,加硫酸酸化,再加过量KI溶液。
③往步骤②所得溶液加入某指示剂,用Na2S2O3滴定至终点(2S2O32- +I2=S4O62- +2I-),记录Na2S2O3溶液用量,平行滴定3次。
(1)步骤①中必须使用的玻璃仪器有烧杯、玻璃棒、和。
(2)完成并配平步骤②中的离子反应:Cr2O72-+ ( )+I- ="=" I2 +Cr3++H2O
(3)步骤③中,指示剂最好选用,该滴定应在接近中性的溶液中进行而不在强酸性溶液进行的原因是。
(4)若3次滴定Na2S2O3溶液的平均用量为12.00mL,则样品的纯度为(Na2S2O3的摩尔质量为158g·mol-1)。
(16分)硅孔雀石是一种含铜矿石,含铜形态为CuCO3·Cu(OH)2和CuSiO3·2H2O,同时含有SiO2、FeCO3、Fe2O3、Al2O3等杂质。以其为原料制取硫酸铜的工艺流程如图:
(1)完成步骤①中稀硫酸与CuSiO3·2H2O反应的化学方程式:
CuSiO3·2H2O+H2SO4=CuSO4 +_______+H2O;双氧水的作用是____。
(2)步骤②调节溶液pH,可以选用的试剂是______。
| A.CuO | B.Fe2O3 | C.Al2O3 | D.Cu(OH)2 |
(3)有关氢氧化物开始沉淀和完全沉淀的pH如下表:
| 氢氧化物 |
Al(OH)3 |
Fe(OH)3[来 |
Fe(OH)2 |
Cu(OH)2 |
| 开始沉淀的pH |
3.3 |
1.5 |
6.5 |
4.2 |
| 沉淀完全的pH |
5.2 |
3.7 |
9.7 |
6.7 |
步骤②中,调节pH=4时,所得滤渣B的成分的化学式为,滤液B中除Cu2+外, 还含有的金属阳离子是。
(4)将滤液B通过、,过滤等操作可得到硫酸铜晶体。
测定硫酸铜晶体结晶水的含量时,应将其放入______中灼烧。加热失水后,若在空气中冷却称量,测定结果_____(填“偏高”、“偏低”或“不变”)。
某小组以醋酸为例探究弱酸的性质。
(1)实验一:探究酸的强弱对酸与镁条反应速率的影响。
①设计实验方案如下表,表中c =________mol·L-1。
| 编号 |
酸的种类 |
酸的浓度/mol·L-1 |
酸的体积/mL |
镁条质量/g |
| 1 |
醋酸 |
1.0 |
10 |
2.0 |
| 2 |
盐酸 |
c |
10 |
2.0 |
②实验步骤:a)检查装置(如图)的气密性后,添加药品;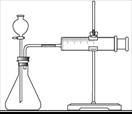
b)反应开始后,________;
c)将所记录的数据转化为曲线图(下图).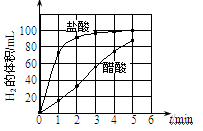
③写出0~5min醋酸、盐酸与镁条反应的反应速率变化规律:________。
(2)实验二:现有一瓶醋酸溶液,常温下测定其中醋酸的电离程度(已电离的电解质分子数占原来总分子数的百分比)。设计实验方案,将待测物理量和对应的测定方法填写在下表中。
| 待测物理量 |
测定方法 |
| ①__________ |
量取25.00ml醋酸溶液于锥形瓶中,滴加指示剂,将0.1000mol·L-1 NaOH标准溶液装入________,滴定至终点,记录数据.重复滴定2次. |
| ②__________ |
__________ |
氯化法是合成硫酰氯(SO2Cl2)的常用方法,实验室合成硫酰氯(SO2Cl2)的反应和实验装置如下:SO2(g)+Cl2(g)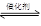 SO2Cl2(l) △H=-97.3kJ/mol。
SO2Cl2(l) △H=-97.3kJ/mol。
有关信息如下:硫酰氯通常条件下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。回答下列问题:
(1)装置甲中仪器A的名称为______,甲中活性炭的作用是________,B的作用为;
(2)装置丁中发生反应的离子方程式为;
(3)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为,分离产物的方法是(填字母);
| A.重结晶 | B.过滤 | C.蒸馏 | D.萃取 |
(4)装置丙的作用为,若缺少装置乙,氯气和二氧化硫可能发生反应的化学方程式为;
(5)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有(填序号)。
①先通冷凝水,再通气 ②控制气流速率,宜慢不宜快
③若三颈烧瓶发烫,可适当降温 ④加热三颈烧瓶