工业上为了使原料和能量得到充分的利用,常常采用循环操作。
Ⅰ、利用热化学循环制氢能缓解能源矛盾。最近研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢。
MnFe2O4的制备:
| |
开始沉淀 |
完全沉淀 |
| Fe3+ |
2.7 |
3.7 |
| Mn2+ |
8.3 |
10.4 |
已知Fe3+、Mn2+沉淀的pH如右表所示。
(1)此工艺中理论上投入原料Fe(NO3)3和Mn(NO3)2的物质
的量之比应为 __________。
(2)控制pH的操作中m的值为 。
Ⅱ、用MnFe2O4热化学循环制取氢气:

(3)由上可知,表示H2燃烧热的热化学方程式是__________________________ 。
(4)该热化学循环制取氢气的优点是_______________(填字母编号)。
A.过程简单、无污染
B.物料可循环使用
C.氧气和氢气在不同步骤生成,安全且易分离
Ⅲ、工业上可用H2、HCl在一定条件下通过下图的循环流程制取太阳能材料高纯硅。
(5)上图中,假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率和反应②中H2的利用率均为75%。则在下一轮次的生产中,需补充投入HCl和H2的体积比是___________________。
A、B、C、D,E和F是六种短周期元素,它们的原子序数依次增大。 A和D,C与F为同主族元素;A的单质是最轻的气体; B元素最高价氧化物的水化物与其气态氢化物反应生成盐; E元素是地壳中含量最多的金属元素。F元素原子M层上电子数比L层少2个电子。试完成下列填空
(1)E元素位于周期表的第周期族。
(2)F简单阴离子的结构示意图。
(3)A、C、D 三种元素共同形成的化合物的电子式,其微粒间存在的化学键有。
(4)铜与B元素最高价氧化物的水化物的稀溶液反应的离子方程式为。
(5)E的硫酸盐溶液中滴入B元素气态氢化物的水溶液,直至过量。离子方程式为。
A、B、C、D、E是中学化学中常见的无色气体,它们均由短周期元素组成。A、B、C相互转化关系如图所示(部分产物已略去)。已知: A能使湿润的红色石蕊试纸变蓝;C、D为空气中的主要成分;B、E是有毒气体,都能和血红蛋白结合。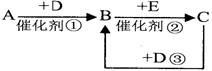
回答下列问题:
(1)A的结构式,C的电子式。
(2)下列气体实验室制取装置与用氯化铵和碱石灰加热制取A的装置相同的是(填序号)。
①氧气②氯气③氢气④二氧化碳
(3)反应②可用于汽车加装尾气催化净化装置,可以使B和E转化成无毒的气体,试写出反应②的化学方程式:。
(4)反应①的化学方程式:。
①14N②金刚石③14C④乙醇(CH3CH2OH)⑤13C⑥二甲醚(CH3OCH3)
(1)和互为同位素(填序号)
(2)和的质量数相同,质子数不同。(填序号)
(3)④和⑥互为。
(4)②金刚石属于晶体,熔化时需要克服微粒间的作用力是。
A、B、C、D、E是位于短周期的主族元素。已知:
①热稳定性:HmD>HmC;
②Cm-、E(m-1)-具有相同的电子层结构;
③A、B与C在同一周期,在该周期元素中,A的原子半径最大,B的离子半径最小;
④A与B质子数之和是D质子数的3倍。
依据上述信息用相应的化学用语回答下列问题:
考查原子核外电子的排布规律及元素周期律等。
(1)HmDm的电子式为
(2)Cm-、E(m-1)-的还原性强弱顺序为:_________,(用离子符号表示)能证明其还原性强弱的离子方程式为________________________________。
(3)B单质与A的最高价氧化物对应水化物反应的化学方程式为:______________________。
(4)常温下,将CDm通入HmC溶液中,有C析出,写出该过程的化学方程式。
(5)在A、B、C、E单质中,符合下列转化关系的是_____________(填元素符号)。
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)。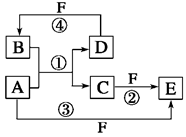
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A 是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A原子的结构示意图为,反应④的化学方程式为_______________。
(2)若A是常见的变价金属的单质,D、F是气态单质,且反应①和②均在水溶液中进行,写出反应②的离子方程式_________,E与A再生成C的离子方程式是。
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为___________________________________。