在碱存在的条件下,卤代烃与醇反应生成醚(R-O-R′):
化合物A经下列四步反应可得到常用溶剂四氢呋喃,反应框图如下: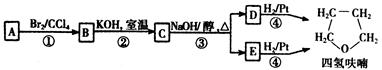
请回答下列问题:
(1)1 mol A和1 mol H2在一定条件下恰好反应,生成饱和一元醇Y,Y中碳元素的质量分数约为65%,则Y的分子式为 __________________________
A分子中所含官能团的名称是 __________________________
A的结构简式为__________________________。
(2)第①②步反应类型分别为① _____________ ② _____________。
(3)化合物B具有的化学性质(填写字母代号)是 _____________。
a.可发生氧化反应 b.强酸或强碱条件下均可发生消去反应
c.可发生加成反应 d.催化条件下可发生加聚反应
(4)写出C、D和E的结构简式:
C _____________ D ___________________E_____________
(5)写出化合物C与NaOH水溶液反应的化学方程式:
_____________________________________________________________________________
(6)写出四氢呋喃链状醚类的所有同分异构体的结构简式:
_____________________________________________________________________________
____________________________________________________________________________
在一容积固定的密闭容器中进行的反应:N2(g)+3H2(g)≒2NH3(g),,达到平衡状态的标志是
①单位时间内生成n m ol N2的同时生成2n mol NH3
ol N2的同时生成2n mol NH3
②氨的生成速率与氨的分解速率相等
③用N2、H2、NH3的物质的量浓度变化表示的反应速率的比为1∶3∶2的状态
④N2、H2、NH3浓度相等
⑤断开1个N≡N键的同时有6个N-H键形成
⑥混合气体的密度不再改变的状态
⑦混合气体的压强不再改变的状态
⑧混合气体的平均相对分子质量不再改变的状态
⑨反应放出的热量等于反应吸收的热量
(4分)非金属元素R,其单质4.8g在氧气中充分燃烧生成RO29.6g,在R原子中,核内质子数等于中子数,则R的元素名称为,其最高价为,与上下左右相邻元素比较,R的最高价氧化物的水化物酸性比弱。用 形式表示该元
形式表示该元 素的原子。
素的原子。
下列反应中,属于放热反应的是,属于吸热反应的是
①燃烧②炸药爆炸③酸碱中和④二氧化碳通过炽热的碳⑤食物因氧化而腐败
⑥Ba(OH)2·8H2O与NH4Cl的反应⑦铁粉与稀盐酸反应
在4L体积不变的密闭 容器中充入6molA气体和5molB气体,发生反应:
容器中充入6molA气体和5molB气体,发生反应:
3A (g) + B (g) 2C (g) + x D (g), 2分钟后反应达到平衡,生成了2molC,经测定D的浓度为0.25mol·L-1, 求:
2C (g) + x D (g), 2分钟后反应达到平衡,生成了2molC,经测定D的浓度为0.25mol·L-1, 求:
(1) x= 。
(2) 用B表示的2分钟内的平均反应速率______________________。
(3)达到平衡时 ,在相同温度下容器内混合气体的压强与反应前压强比为。
,在相同温度下容器内混合气体的压强与反应前压强比为。
(4)达到平衡状态时B的转化率为。
右下图是以Zn和Cu为电极,稀硫 酸为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
酸为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
| Date:2011.03.06 实验后的记录: ①Zn为阳极,Cu为阴极 ②H+向负极移动 ③电子流动方向Zn→Cu ④Cu极有H2产生 ⑤若有1mol电子流过导线,则产生H2为0.5mol。 ⑥正极的电极反应式:Zn-2e- =Zn2+ |
(1)在卡片上,叙述合理的是__________________(填序号)。
(2)在实验中,甲同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是__ __________________________________________________。
__________________________________________________。
(3)如果把锌片换成石墨,发现电流计指针几乎不能偏转,原因________________。
(4)如果把硫酸换成硫酸铜溶液,猜测_________(填“锌极”或“铜极”)变粗,原因是__________________(用电极方程式表示)。