下面是某高分子有机物的合成路线,Ⅲ、V为Ⅵ的单体。
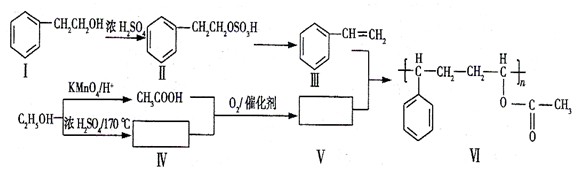
回答下列问题:
(1) 由Ⅱ生成Ⅲ的反应类型名称为 。
(2)下列关于化合物I、Ⅱ和Ⅲ的说法中,正确的是 (填字母)。
A.化合物I可以发生氧化反应 B.化合物I不能与Na反应生成氢气
C.从I→Ⅱ和Ⅱ→Ⅲ两反应来看,I→Ⅲ过程中浓硫酸有催化剂的作用
D.化合物Ⅲ与HCl加成,只能生成一种有机产物
(3)化合物V是 (填字母)类化合物。
A.醇 B.烷烃 C.烯烃 D.酸 E.酯
(4)在上述合成路线中,化合物Ⅳ和CH3COOH在催化剂的作用下与氧气反应生成V和水,写出反应方程式 。
(5)下图为分离化合物V、乙酸和乙醇混合物的实验操作流程图:
在上述实验过程中,所涉及的三次分离操作分别是 。
A.①蒸馏②过滤③分液 B.①分液②蒸馏③蒸馏
C.①蒸馏②分液③分液 D.①分液②蒸馏③结晶、过滤
(6)写出I的同分异构体中能让FeCl3溶液显紫色的任意一种结构简式:
。
(7)写出反应III+V→VI的化学方程式:(不要求写反应条件)
。
(11分)2SO2(g)+O2(g)  2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 molSO3(g)的ΔH=-99 kJ/mol。
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 molSO3(g)的ΔH=-99 kJ/mol。
请回答下列问题:
(1)图中A、C分别表示_____ ___、____ ____,E的大小对该反应的反应热有无影响?________.该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________,理由是_____________________________。
(2) 图中ΔH=_____ ___kJ/mol.
(3) V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化.写出该催化循环机理的化学方程式:_______________________
_______________________________________________。
(4)如果反应速率v(SO2)为0.05 mol/(L·min),则v(O2)=__________mol/(L·min)、v(SO3)=________ mol/(L·min).
(5) 已知单质硫的燃烧热为296 kJ/mol,计算由S(s)生成3 mol SO3(g)的ΔH=。
在同温同压下,同体积的CH4和CO2分子数之比为,物质的量之比为,原子总数之比为,质量之比为,密度之比为。
CO2的摩尔质量是;2molCO2的质量是;它在标准状况下所占的体积约为,所含的分子数目约为;所含氧原子的数目约为。
(共8分)
在2 L恒容密闭容器中,800 ℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
| 时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
| n(NO)(mol) |
0.020 |
0.010 |
0.008 |
0.007 |
0.007 |
0.007 |
(1)如图中表示NO2的变化的曲线是。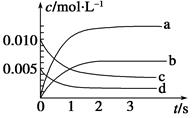
(2)求 2 s末用氧气表示的平均反应速率v(O2)=
(3)求达平衡时NO的转化率为
(4)能说明该反应已经达到平衡状态的是。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v(NO)逆=2v(O2)正d.容器内的密度保持不变
(5)能够使该反应的反应速率增大,且平衡向正反应方向移动的是。
a.及时分离出NO2气体 b.增大O2的浓度
(共10分)
(1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ·mol-1表示。请认真观察下图,然后回答问题。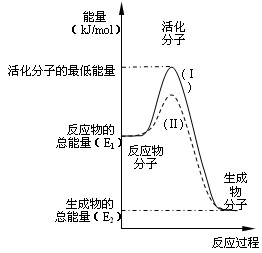
①图中所示反应是(填“吸热”或“放热”)反应,该反应(填“需要”、“不需要”或“不一定”)加热,该反应的△H =(用含E1、E2的代数式表示)。
②对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,活化分子百分数增多,反应速率加快,你认为最可能的原因是____________________________________。
(2)把煤作为燃料可通过下列两种途径:
途径Ⅰ ①C(s)+O2(g) === CO2(g) ΔH1<0
途径Ⅱ 先制水煤气:②C(s)+H2O(g) === CO(g)+H2(g) ΔH2>0
再燃烧水煤气:
③2CO(g)+O2(g) === 2CO2(g) ΔH3<0④2H2(g)+O2(g) === 2H2O(g) ΔH4<0
请回答下列问题:
①判断两种途径放热:途径Ⅰ放出的热量________途径Ⅱ放出的热量(填“大于”、“等于”或“小于”)。
②ΔH1、ΔH2、ΔH3、ΔH4的数学关系是_________________________________。
③由于制取水煤气的反应里,反应物具有的总能量________(填“大于”“等于”或“小于”)生成物具有的总能量,那么在化学反应时,反应物就需要________能量才能转化为生成物,因此其反应条件为________。
(3)已知:Fe2O3(s)+3CO(g) === 2Fe(s)+3CO2(g) ΔH1=-25 kJ·mol-1①
3Fe2O3(s)+CO(g) === 2Fe3O4(s)+CO2(g)ΔH2=-47 kJ·mol-1②
Fe3O4(s)+CO(g) === 3FeO(s)+CO2(g)ΔH3=+19 kJ·mol-1③
请写出CO还原FeO的热化学方程式:______________________________________。