将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是
| A.镁比铝活泼,镁失去电子被氧化成Mg2+ |
| B.铝是电池负极,开始工作时溶液中会立即有白色沉淀生成 |
| C.该装置开始工作时,铝片表面的氧化膜可不必处理 |
| D.装置的内外电路中,均是电子的定向移动形成电流 |
下列有机物的化学式与名称对应不正确的是
A.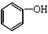 石炭酸 石炭酸 |
B.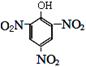 TNT TNT |
| C.HCOOH 蚁酸 | D.CH2BrCH2Br 1,2—二溴乙烷 |
上海环保部门为了使城市生活垃圾得到合理利用,近年来逐步实施了生活垃圾分类投放的办法。其中塑料袋、废纸、旧橡胶制品等属于
| A.无机物 | B.有机物 | C.盐类 | D.非金属单质 |
下列物质中,没有固定沸点的是
| A.聚乙烯 | B.氯仿 | C.甲苯 | D.异丁烷 |
氰化物有剧毒,在碱性条件下可用如下方法进行处理: 。下列判断错误的是
。下列判断错误的是
A.上述反应中的氧化剂是 |
B.还原性: > > |
C.当有0.2 生成时,溶液中阴离子的物质的量增加1 生成时,溶液中阴离子的物质的量增加1 |
D.经测定 的水溶液呈碱性,说明 的水溶液呈碱性,说明 促进了水的电离 促进了水的电离 |
某化学小组研究在其他条件不变时,改变密闭容器中某一条件对
 化学平衡状态的影响,得到如下图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是
化学平衡状态的影响,得到如下图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是
A.在 和 和 不变时达到平衡, 不变时达到平衡, 的物质的量大小为:c>b>a 的物质的量大小为:c>b>a |
B.若 > > ,则正反应一定是放热反应 ,则正反应一定是放热反应 |
C.达到平衡时 的转化率大小为:b>a>c 的转化率大小为:b>a>c |
D.若 > > ,达到平衡时b、d点的反应速率为 ,达到平衡时b、d点的反应速率为 > > |