以下是有关SO2、Cl2的性质实验。
(1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质。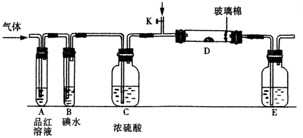
①若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同? (填“相同”或“不相同”);若置D装的是铁粉,通入Cl2与铁粉充分反应时现象为
;若装置D中装的是五氧化二钒(催化剂)。通入SO2时,打开K通入适量O2的化学反应方程式为 。
②若装置B中装有5.0 mL 1.0×10-3mol/L在碘水,当通入足量Cl2完全反应后,共转移了5.0×10-5mol电子,该反应的化学方程式为 。
③E中盛有 溶液。
(2)某同学将足量的SO2通入一支装有氧化钡溶液的试管,未见沉淀生成,若向该试管中加入加量(填字母) ,则可以看到白色沉淀产生。
| A.氨水 | B.稀盐酸 | C.稀硝酸 | D.氯化钙 |
(3)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4∶3;当Cl2的与含X的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式 。
I下列实验操作或对实验事实的描述中正确的是_______________
①石油的分馏实验必须将温度计的水银球插入反应液中,测定反应液的温度,其中冷凝管起到冷凝回流的作用
②将0.1mol•L﹣1的NaOH溶液与0.5mol•L﹣1的CuSO4溶液等体积混合制得氢氧化铜浊液,用于检验醛基
③不慎将苯酚溶液沾到皮肤上,立即用酒精清洗
④配制银氨溶液:在一定量AgNO3溶液中滴加过量氨水即可
⑤分离苯和苯酚的混合液,加入少量浓溴水,过滤
⑥将10滴溴乙烷加入1mL10%的烧碱溶液中加热片刻后,再滴加2滴2%的硝酸银溶液,以检验水解生成的溴离子.
II某校学生为探究苯与溴发生反应的原理,用如图装置进行实验.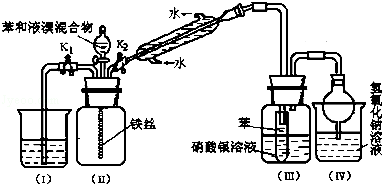
根据相关知识回答下列问题:
(1)实验开始时,关闭K1,开启K2和分液漏斗活塞,滴加苯和液溴的混合液,反应开始.过一会儿,在(Ⅲ)中可能观察到的现象是____________________________________
(2)整套实验装置中能防止倒吸的装置有________________(填装置序号).
(3)反应结束后要使装置(I)中的水倒吸入装置(Ⅱ)中.这样操作的目的是______________________
(4)你认为通过该实验后,有关苯跟溴反应的原理方面能得出的结论是_______________________
(每空2分,共12分)实验室以草酸(HOOC—COOH)和乙醇为原料制备草酸二乙酯的实验步骤如下:
步骤1:在上图所示装置中,加入无水草酸45g,无水乙醇81g,苯200mL,浓硫酸10mL,搅拌下加热68-70℃回流共沸脱水。
步骤2:待水基本蒸完后,分离出乙醇和苯。
步骤3:所得混合液冷却后依次用水、饱和碳酸氢钠溶液洗涤,再用无水硫酸钠干燥。
步骤4:常压蒸馏,收集182-184℃的馏分,得草酸二乙酯57g。
(1)步骤1中发生反应的化学方程式是,反应过程中冷凝水应从(填“a”或“b”)端进入。
(2)步骤2操作为。
(3)步骤3用饱和碳酸氢钠溶液洗涤的目的是。
(4)步骤4除抽气减压装置外所用玻璃仪器有蒸馏烧瓶、冷凝管、接液管、锥形瓶和。
(5)本实验中,草酸二乙酯的产率为。
工业上测量SO2、N2、O2混合气体中SO2含量的装置如下图;反应管中装有碘的淀粉溶液。SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2+2H2O→H2SO4+2HI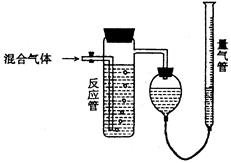
(1)混合气体进入反应管后,量气管内增加的水的体积等于的体积(填写气体的分子式)。
(2)反应管内溶液蓝色消失后,没有及时停止通气,则测得的SO2含量(选填:偏高,偏低,不受影响)。
(3)反应管内的碘的淀粉溶液也可以用代替(填写物质名称)。
(4若碘溶液体积为VamL.,浓度为Cmol·L-1,N2与O2的体积为VbmL(已折算为标准状况下的体积)。用C.Va.Vb表示SO2的体积百分含量为:。
(5)将上述装置改为简易实验装置,除导管外,还需选用的仪器为.(选下列仪器的编号)。
a.烧杯
b.试管
c.广口瓶
d.容量瓶
e.量筒
f.单孔塞
g.双孔塞
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用下图所示的装置制取乙酸乙酯。回答下列问题:
(1)写出制取乙酸乙酯的化学反应方程式
(2)饱和碳酸钠溶液的主要作用是。
| A.中和乙酸 | B.吸收乙醇 |
| C.降低酯的溶解度使分层清晰 | D.有利于酯的水解 |
(3)若要把制得的乙酸乙酯分离出来,应采用的实验操作是。
(4)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有。(填序号)
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
某小组同学要配制100 mL 0.100 mol·L-1 Na2CO3溶液。下图是一些关键步骤和操作。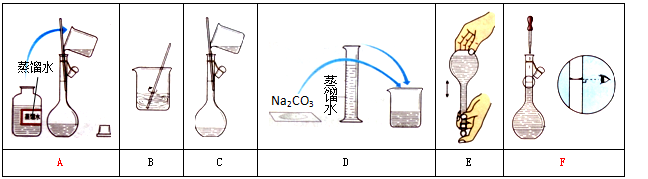
(1)配制过程的先后顺序为(用字母A~F填写)。
(2)配制过程所需的玻璃仪器有烧杯、玻璃棒、量筒、。
(3)若用Na2CO3·10H2O晶体来配制溶液,需要称量固体,但晶体已经部分失去结晶水,则所配得溶液的浓度会(填“偏高”、“偏低”、“不变”)。
(4)步骤A通常称为洗涤,如果没有步骤A,则配得溶液的浓度将(填“偏高”、“偏低”、“不变”);步骤F称为,如果俯视刻度线,配得溶液的浓度将(填“偏高”、“偏低”、“不变”)。
(5)在步骤B之后,需才进行下一步操作。