、、、、是原子序数依次增大的短周期主族元素,、在周期表中的相对位置如右表;元素最低负化合价的绝对值与其原子最外层电子数相等;是地壳中含量最多的金属元素。
(1)的离子结构示意图为;元素在周期表中位于第族。
(2)和氢组成的化合物分子有6个原子,其结构简式为。
(3)和形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为
(4)的最简单气态氢化物甲的水溶液显碱性。
①在微电子工业中,甲的水溶液可作刻蚀剂的清除剂,所发生反应的产物不污染环境,其化学方程式为。
②一定条件下,甲在固定体积的密闭容器中发生分解反应(>0)并达平衡后,仅改变下表中反应条件,该平衡体系中随递增递减的是(选填序号)。
| 选项 |
||||
| 温度 |
温度 |
加入的物质的量 |
加入甲的物质的量 |
|
| 甲的物质的量 |
平衡常数K |
甲的转化率 |
生成物物质的量总和 |
(5)由、形成的液态化合物0.2在中完全燃烧,生成两种气态氧化物,298时放出热量215。 该反应的热化学方程式为。
工业上制各硝酸的第一步反应是
4NH3+5O2 4NO+6H2O
4NO+6H2O
某化学课外小组设计了如图所示的实验装置,模拟进行该实验。图中箭头表示气体流向。A表示一种纯净、干燥的气体,B是另一种气体,反应进行一段时间后,装置己中有红棕色气体生成。
实验中所用的药品和干燥剂只能从下列物质中选取:Na2CO3、NaHCO3、MnO2、Na2O2、NaCl、无水CaCl2、NH4HCO3、碱石灰等固体和双氧水、蒸馏水。(戊中电阻丝为铂丝,反应开始后断开K)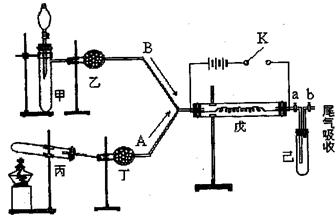
根据图中装置和反应现象请回答:
(1)丙中发生反应的化学方程式为:;
丁中的干燥剂应选:
(2)甲中发生反应的化学方程式为:____。
(3)戊中发生的主要反应是反应(填“吸热”或“放热”),可能发生的什么现象可以证明你的判断?
(4)当己中充满红棕色气体后,停止给丙加热,并关闭a、b两个活塞,若将己浸入冰水中,则己中会出现的现象是,简述产生此现象的原因。
(一)元素X、Y、Z和W的质子数依次增大,都不超过20。X的原子半径是元素中最小的,Z元素的非金属性是元素中最强的,Y原子的最外层达到稳定结构所需的电子数恰好等于内层的电子数。W元素的原子结构中,K层、L层的电子数之和等于M层、N层的电子数之和。
请用文字和化学用语回答下列问题:
(1) X2Y分子形状是,是____分子(填“极性”或“非极性”)。
(2)用电子式表示化合物WZ2的形成过程。
XZ在X2Y中可以任意比例溶解,原因是。
(3)写出由这些元素组成的物质之间发生的一个置换反应。
(二)氮是地球上含量丰富的一种元素,氮及其化合物在工量农业生产、生活中有着重要作用。请回答下列问题:
右图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式。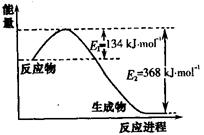
归纳整理是科学学习的重要方法之一。在学习了氧族元素的各种性质后,可归纳整理出如下表所示的表格(部分)。
| 性质\元素 |
8O |
16S |
34Se |
52Te |
| 单质熔点(℃ |
—218。4 |
113 |
450 |
|
| 单质沸点(℃) |
—183 |
444.6 |
685 |
1390 |
| 主要化合价 |
—2 |
—2,+4,+6 |
—2,+4,+6 |
|
| 原子半径 |
逐渐增大 |
|||
| 单质与H2反应情况 |
点燃时易化合 |
加热化合 |
加热难化合 |
不能直接化合 |
请根据上表回答下列问题:
(1)晶体硫属于晶体,硒的焙点T的范围可能是。
(2)碲的化合价可能有。
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是(填化学式)。
(4)氢硒酸有较强的(填“氧化性”或“还原性”),因此放在空气中长期保存易变质,其可能发生的化学方程式为。
(5)工业上Al2Te3可用来制各H2Te,完成下列化学方程式:
Al2Te3+()一A1(OH)3↓+H2Te↑
将a mol Na2O2与b mol NaHCO3混合共热到300℃,充分反应后(不与外界物质发生反应)得到固体和气体的成分,随着a与b的比值不同而不同,当a与b的比值为下列数值时,把得到的固体和气体的化学式填入下表:
| a/b |
固体物质的成分 |
气体物质的成分 |
| <1/2 |
||
| =1/2 |
||
| =1/1 |
||
| >1/1 |
现有甲、乙两瓶无色溶液,已知它们可能是NaOH溶液和AlCL3溶液。现做如下实验:
①440mL甲溶液与120mL乙溶液反应,产生1.56沉淀
②120mL甲溶液与440mL乙溶液反应,产生1.56沉淀
③120mL甲溶液与400mL乙溶液反应,产生3.12沉淀
通过必要的计算和推理判定:
甲溶液是_______,其浓度为____mol/L。乙溶液是_______其浓度为____mol/L