接触法制硫酸工艺中,其主反应在并有催化剂存在下进行:
1)该反应所用的催化剂是(填写化合物名称),该反应时的平衡常数时的平衡常数(填"大于"、"小于"或"等于").
2)该热化学反应方程式的意义是.
3)达到化学平衡状态的是
a. b.容器中气体的平均分子量不随时间而变化
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
4)在一个固定容积为5L的密闭容器中充入和,半分钟后达到平衡,测得容器中含,则:若继续通入和,则平衡移动(填"向正反应方向"、"向逆反应方向" 或"不"),再次达到平衡后,mol<<mol。
根据要求填空:
(1)写出下列原子团的电子式:①甲基②羟基
(2)写出下列有机物的键线式:
 ___________ CH3CH2CH2COOH _________
___________ CH3CH2CH2COOH _________
(3) 写出有机物
写出有机物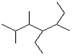 的名称
的名称
(4)某有机高分子化合物的结构片段如下: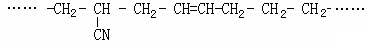
则合成它的单体是。
(5)分子式为C8H8O2,符合下列条件的同分异构体共有种。
①含有 结构②含有苯环,苯环上只有一个侧链。
结构②含有苯环,苯环上只有一个侧链。
已知固体草酸(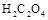 )分解的化学方程式为:
)分解的化学方程式为: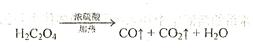
某实验小组为测定铁锈样品的组成(假定铁锈中只有 和
和 两种成份),利用草酸分解产生的CO和铁锈反应,实验装置如下图所示。
两种成份),利用草酸分解产生的CO和铁锈反应,实验装置如下图所示。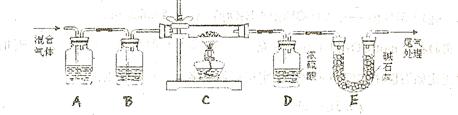
(1)为得到干燥、纯净的CO气体,洗气瓶A、B中盛放的液态试剂依次是、(填答案编号)a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液 d.氯化钙溶液
(2)在点燃C处酒精灯之前应进行的操作是:(a)检查装置气密性;
(b);
(3)E装置的作用是。
上述装置最后尾气处理的方法是:
(4)准确称量样品质量10.00g置于硬质玻璃管中,充分反应后冷却、称量(假设每步均完全反应),硬质玻璃管中剩余固体质量为8.32g,D中浓硫酸增重0.72g,则n=.
(5)在本实验中,下列情况会使测定结果n偏大的是(填答案编号)
a.缺少装置B b.缺少装置E c.反应后的固体剩余少量
糖类物质为很多生物生命活动提供能量。
(1)已知 45g葡萄糖在人体内完全氧化为二氧化碳和水,放出701KJ的热量,该反应的热化学方程式。
(2)以葡萄糖为燃料的微生物燃料电池结构如图所示,其负极反应为: .
电池工作过程中溶液中氢离子移动方向从极区
移向极区(填“正”或“负”)
(3)常温下,用上述电池惰性电极电解100L某浓的硫酸铜溶液,当溶液PH=1时停止电解,则理论上需要葡萄糖的质量为。(假设溶液体积不变)
8分)一定条件下经不同的化学反应,可以实现图示变化,A为酸式盐;B为无色无味气体;无色气体D可使红色石蕊试纸变蓝;X、F和Y为气体单质,且Y为有色气体,F为空气的主要成分之一;G为正盐,G和无色气体M在溶液中可反应生成B。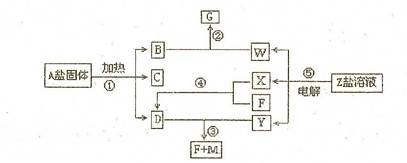
(1)写出下列物质的化学式:A; Y.
(2)写出反应②的离子方程式
(3)写出反应③的化学议程式
(4)常温下PH=10,体积均为100mL的D、W两溶液与M反应,消耗的M的物质的量关系
D W(填“大于”“ 小于”或“等于”)
(18分)1.已知一般钾盐均为可溶性的强电解质。在某溶液中可发生下列反应: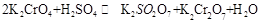
(1)试将上述反应改写成离子议程式
(2)该离子反应的平衡常数表达式为:K=;
(3)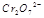 在水溶液中为红色,
在水溶液中为红色, 在水溶液中为黄色。某条件下该反应建立平衡后,体系为两种离子的混合液,颜色为橙色。
在水溶液中为黄色。某条件下该反应建立平衡后,体系为两种离子的混合液,颜色为橙色。
若加水将其稀释,溶液颜色将偏(红、黄)原因是 ;
;
若在在上述平衡体系的溶液中中加入硫酸钾固体体系颜色有何变化?为什么?
Ⅱ.固定和利用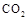 ,能有效地利用资源,并减少空气中的温室气体。工业上正在研究利用
,能有效地利用资源,并减少空气中的温室气体。工业上正在研究利用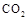 来生产甲醇燃料的方法,该方法的化学方程式是:
来生产甲醇燃料的方法,该方法的化学方程式是: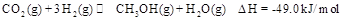
某科学实验将6mol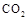 和8molH
和8molH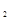 充入一容积为2L的密闭容器中,测得H
充入一容积为2L的密闭容器中,测得H 的物质的量随时间变化如右图中实线所示(
的物质的量随时间变化如右图中实线所示( 图中字母后数字表示对应的坐标):
图中字母后数字表示对应的坐标):
问题:
(1)由图分析,在下列时间段内反应速率最快的时间段是(填答案编号)。
a.0~1min b.1~3min c.3~8min d.8~11min
(2)仅改变某一条件再进行实验,测得H 的物质的量随时间变化如图中虚线所示。与实线相比,曲线Ⅰ改变的条件可能是,曲线Ⅱ改变的条件可能是
的物质的量随时间变化如图中虚线所示。与实线相比,曲线Ⅰ改变的条件可能是,曲线Ⅱ改变的条件可能是
。
(3)下列表述能表示该反应已达平衡的是(填答案编号)
a.容器内压强不再改变 b.容器内气 体的密度不再改变
体的密度不再改变
c.容器内气体平均摩尔质量不再改变 d.容器内各物质的物质的量相等