A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中,A、C及B、D分别是同主族元素;A元素的原子半径是所有主族元素中原子半径最小的;B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的2倍;四种元素所形成的单质中A、B单质是气体,C、D单质是固体。 (1)写出以下元素的名称: B____________;C___________。
(1)写出以下元素的名称: B____________;C___________。 (2)用电子式表示C2D的形成过程:___________。
(2)用电子式表示C2D的形成过程:___________。 (3)由B、C两元素所形成的原子个数比为1:1的化合物属于__________(填“离子” 或“共价”)化合物,存在的化学键的种类有________(若有共价键需要写出具体的共价键类型),写出它与水反应的离子方程式____ 。
(3)由B、C两元素所形成的原子个数比为1:1的化合物属于__________(填“离子” 或“共价”)化合物,存在的化学键的种类有________(若有共价键需要写出具体的共价键类型),写出它与水反应的离子方程式____ 。 (4)实验室常用A、B两元素所形成的原子个数为1:1的化合物来制备一种常见气体,写出实验室中用固体药品制备该气体的的化学方程式______________。
(4)实验室常用A、B两元素所形成的原子个数为1:1的化合物来制备一种常见气体,写出实验室中用固体药品制备该气体的的化学方程式______________。
(5)写出B的原子结构示意图 若一个B原子中有8个中子,写出B的原子符号
(6)写出均由A、B、C、D四种元素组成的两种物质之间发生反应的离子方程式
(7)由A、B两元素形成的单质在以铂作电极稀硫酸作电解液形成的燃料电池中,正极的电极方程式为 ,若以氢氧化钾为电解液则负极的电极方程式为 。
(1)写浓盐酸与二氧化锰加热反应来制取氯气的化学方程式。
(2)写出氢氧化钡溶液与稀硫酸反应的离子方程式。
甲、乙、丙、丁分别是盐酸、碳酸钠、氯化钙、硝酸银4 种溶液中的一种。将它们两两混合后,观察到的现象是:
①甲与乙或丙混合都产生沉淀;
②丙与乙或丁混合也产生沉淀;
③丁与乙混合产生无色气体。回答下面问题:
(1)写出丁与乙反应的离子方程式:。
(2)这四种溶液分别是:甲:、乙:、丙:、丁:
(1)将下列离子Na+、K+、Cu2+、H+、NO3-、Cl-、CO32-、OH-按可能大量共存于同一溶液的情况,把他们分成A、B两组,而且每组中均含两种阳离子和两种阴离子。
A组:。
B组:。
(2)写出下列反应的离子方程式
氧化铁和稀硫酸反应
碳酸氢钠溶液和足量澄清石灰水反应
氢氧化铜溶解与稀硫酸
碳酸钙和醋酸溶液
(9分) 向一体积不变的密闭容器中加入2 mol A、0.6 mol C和一定量的B三种气体。
一定条件下发生反应,各物质浓度随时间变化如图1所示。图2为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。
已知t3-t4阶段为使用催化剂;图1中t0-t1阶段c(B)未画出。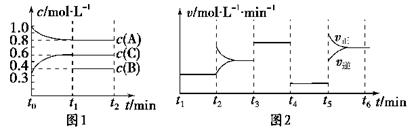
(1)若t1=15 min,则t0-t1阶段以C浓度变化表示的反应速率为v(C)=________。
(2)t4-t5阶段改变的条件为________,B的起始物质的量为________。各阶段平衡时对应的平衡常数如下表所示:
| t1~t2 |
t2~t3 |
t3~t4 |
t4~t5 |
t5~t6 |
| K1 |
K2 |
K3 |
K4 |
K5 |
则K1=________(保留两位小数),K1、K2、K3、K4、K5之间的关系为________(用“>”“<”或“=”连接)。
(3)t5-t6阶段保持容器内温度不变,若A的物质的量共变化了0.01 mol,而此过程中容器与外界的热交换总量为a kJ,写出此温度下该反应的热化学方程式:________________________。
(4)在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,达到平衡时体系中各物质的量与t1时刻相等,a、b、c要满足的条件为________。
(1)肼(N2H4)又称联氨,是一种可燃性液体,可用作火箭燃料。已知在101kPa,320g N2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧的热化学方程式是:
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20~30%的KOH溶液。肼—空气燃料电池放电时,正极的电极反应式是;负极的电极反应式是。
(3)如图是一个电化学过程示意图。假设使用肼—空气燃料电池作为本过程的电源,铜片质量变化128g,则肼—空气燃料电池理论上消耗标准状况下的空气L(假设空气中氧气的体积含量为20%)。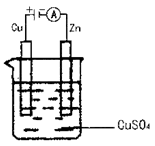
(4)传统制备肼的方法是以NaClO氧化NH3制得肼的稀溶液,该反应的离子方程式是。