下图转化关系中,A、B、C、D、E都是短周期元素的单质,在常温常压下A是固体,其余都是气体,且C呈黄绿色。化合物H和I两种气体相遇时产生白烟。化合物G的焰色反应为黄色。反应①和②均在溶液中进行。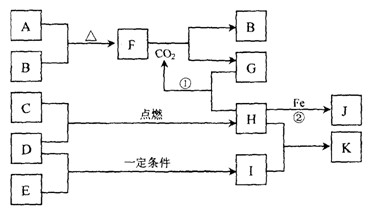
请按要求回答下列问题。
(1)写出下列物质的化学式D 、F
(2)反应①的离子方程式为 。
(3)向K溶液中加入硝酸酸化的硝酸银溶液,反应的现象为 。
(4)将少量单质C通入盛有淀粉KI溶液的试管中,液体变为蓝色。该反应的离子方程式为 。这说明单质C的氧化性 于单质碘(填“强”或“弱”)。
恒温下,将amol N2与bmol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g) 2NH3(g)
2NH3(g)
计算过程:
(1)若反应进行到某时刻t时,nt(N2)=8mol,nt(NH3)=4mol,计算a的值。
(2)反应达平衡时,混合气体的体积为537.6 L(标准状况下),其中NH3的体积分数为25%。求原混合气体中,a∶b=________。
(3)平衡混合气体中,n(N2)∶n(H2)∶n(NH3)=________。
恒温下,将amol N2与bmol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g) 2NH3(g)
2NH3(g)
计算过程:
(1)若反应进行到某时刻t时,nt(N2)=8mol,nt(NH3)=4mol,计算a的值。
(2)反应达平衡时,混合气体的体积为537.6 L(标准状况下),其中NH3的体积分数为25%。求原混合气体中,a∶b=________。
(3)平衡混合气体中,n(N2)∶n(H2)∶n(NH3)=________。
对于反应:N2(g)+3H2(g)  2NH3(g) ΔH<0
2NH3(g) ΔH<0
(1)能使正反应速率瞬时加快的因素有____________(填字母,下同);
(2)能使逆反应速率瞬时加快的因素有____________
| A.增大N2和H2的浓度 |
| B.增大压强 |
| C.升高温度 |
| D.加(正)催化剂 |
E.增加NH3浓度
F.减少NH3浓度
在体积不变的密闭容器里,通入x mol H2(g)和y mol I2(g),发生反应:
H2(g)+I2(g) 2HI(g)△H<0
2HI(g)△H<0
改变下列条件后,反应速率将如何改变?(填“增大”“减小”或“不变”)
(1)升高温度 ;(2)加入催化剂 ;
(3)充入更多的H2 ;(4)容器容积不变,通入氖气 。
(1)已知:C2H6O(g) + 3O2(g) ="=" 2CO2(g) + 3H2O(g)△H1
H2O(g)==H2O(l)△H2 ;
C2H6O(g)==C2H6O(l)△H3
若使1mol C2H6O(l)完全燃烧生成液态水,则放出的热量为 (用符号表示)
(2)对于可逆反应CO(g)+H2O (g)  CO2(g)+H2 (g),若开始时容器中各有1mol的CO(g)和H2O (g),并在一定条件下发生反应,回答下面的问题:
CO2(g)+H2 (g),若开始时容器中各有1mol的CO(g)和H2O (g),并在一定条件下发生反应,回答下面的问题:
①恒温恒压时,向容器中充入0.5mol的He,这时反应速率 (填“加快”、“减慢”或 “不变”),原因是 。
②恒温恒容时,加入0.3mol的CO,这时反应速率 (填“加快”、“减慢”或 “不变”),原因是 。