对于反应:2SO2+O2 2SO3,当其他条件不变时,只改变一个反应条件,将生成SO3的反应速率的变化填入空格里(填写“增大”“减小”“不变”)
2SO3,当其他条件不变时,只改变一个反应条件,将生成SO3的反应速率的变化填入空格里(填写“增大”“减小”“不变”)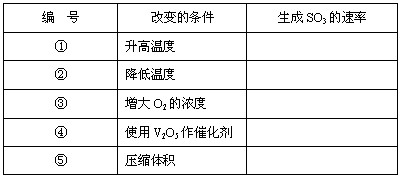
如图所示水槽中试管内有一枚铁钉,放置数天观察: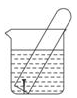
(1)铁钉在逐渐生锈,则铁钉的腐蚀属于____________腐蚀。
(2)若试管内液面上升,则原溶液是____________性,发生____________腐蚀,电极反应:负极:____________,正极____________。
(3)若试管内液面下降,则原溶液呈____________,发生____________腐蚀,电极反应:负极____________,正极____________。
在由铜片、锌片和200 mL稀H2SO4组成的原电池中,若锌片上只发生电化学腐蚀,当在铜片上共放出3.36 L(标准状况)的气体时,H2SO4恰好全部用完,则要产生这些气体需要消耗锌_________g,有_____________mol电子通过导线,原H2SO4溶液的浓度是_____________mol·L-1。
通常情况下,多个羟基连接在同一个碳原子上的分子结构是不稳定的,容易自动失水,生成碳氧双键的结构:
下图是9个化合物的转变关系:
(1)化合物①是____,它跟氯气发生反应的条件A是____。
(2)化合物⑤跟⑦可在酸的催化下去水生成化合物⑨,⑨的结构简式是____,名称是____。
(3)化合物⑨是重要的定香剂,香料工业上常用化合物②和⑧直接合成它。此反应的化学方程式是____。
A、B两种金属元素的相对原子质量之比为8∶9,将A、B两种金属单质按物质的量之比为3∶2组成1.26 g混合物。将此混合物与足量稀硫酸溶液反应,放出1.344 L(标准状况)氢气。若这两种金属单质在反应中生成氢气的体积相等,则A的摩尔质量是 ,B的摩尔质量是 。
(1)根据0.012 kg12C所含的碳原子数约为 ,可以计算出1个12C原子的质量为 。已知1个Fe原子的质量为9.28×10-26kg,可以计算出铁原子的相对质量为 。
(2)9.2 g氮的氧化物NOx中氮原子数为0.2 mol,则NOx的摩尔质量为 ,x的数值为 ,此质量的NOx在标准状况下的体积约为 。