下列叙述不正确的是( )
| A.NH3易液化,液氨常用作制冷剂 |
| B.与金属反应时,稀HNO3可能被还原为更低价态,则稀HNO3氧化性强于浓HNO3 |
| C.铵盐受热易分解,因此贮存氨态氮肥时要密封保存,并放在阴凉通风处 |
| D.稀HNO3和活泼金属反应时主要得到氢气 |
下列物质敞口放置或暴露于空气中,质量增加的是
| A.浓盐酸 | B.浓硫酸 | C.浓硝酸 | D.硅酸 |
未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列符合未来新能源标准的是①天然气 ②煤 ③石油 ④太阳能 ⑤生物质能 ⑥风能 ⑦氢能
| A.①②③④ | B.③⑤⑥⑦ | C.④⑤⑥⑦ | D.③④⑤⑥⑦ |
下列广告语在科学上没有错误的是
| A.这种饮料不含任何化学物质 |
| B.这种口服液含丰富的氮、磷、锌等微量元素 |
| C.这种神奇液体加入水中可以“以水代油”做发动机燃料 |
| D.没有水就没有生命 |
已知:N2(g)+3H2(g) 2NH3(g);△H=-Q kJ·mol-1(Q>0)。现有甲乙两个相同的密闭容器,向甲容器中充入1mol N2(g)和3mol H2(g),在一定条件下达到平衡时放出的热量为Q1 kJ;在相同条件下向乙容器中充入2mol NH3(g),达到平衡时吸收的热量为Q2 kJ。已知Q2=3Q1,下列叙述中正确的是: ( )
2NH3(g);△H=-Q kJ·mol-1(Q>0)。现有甲乙两个相同的密闭容器,向甲容器中充入1mol N2(g)和3mol H2(g),在一定条件下达到平衡时放出的热量为Q1 kJ;在相同条件下向乙容器中充入2mol NH3(g),达到平衡时吸收的热量为Q2 kJ。已知Q2=3Q1,下列叙述中正确的是: ( )
A.Q1= Q Q |
| B.达到平衡时,甲容器中H2的转化率为25% |
C.平衡时甲容器中气体的压强为开始时压强的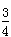 |
| D.平衡时甲容器中NH3(g)的体积分数比乙容器中的小 |
常温下,有下列四种溶液:
| ① |
② |
③ |
④ |
| 0.1mol/L NaOH溶液 |
pH = 11 NaOH溶液 |
0.1mol/L CH3COOH溶液 |
pH = 3 CH3COOH溶液 |
下列说法正确的是( )
A.由水电离出的c(H+):①>③
B.③稀释到原来的100倍后,pH与④相同
C.①与③混合,若溶液pH = 7,则V(NaOH)>V(CH3COOH)
D.②与④混合,若溶液显酸性,则所得溶液中离子浓度可能为: c(CH3COO-)>c(H+)>c(Na+)>c(OH-)