、如下图所示,甲、乙两池电极材料都是铁棒与碳棒,乙池中电子电子流动方向见图,回答下列问题: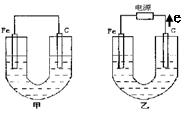
(1)若两池中均盛200mL饱和NaCl溶液和酚酞的混合液,反应开始后:
①甲池中 极,乙池中的
极附近溶液变红(填“正”或“负”或“阴”或“阳”)。
②甲池碳极上电极反应式是
乙池中Fe电极上反应式为 。
③若乙池中收集到1.12L(标况下)有色气体时,停止实验,忽略池中溶液体积的变化,则池中溶液的c(OH—)约为 ,要使溶液恢复到电解前的相同的状况,应向溶液中补充一定量的 
| A.盐酸 | B.NaCl固体 | C.NaCl溶液 | D.HCl气体 |
(2)若两池中均盛有200mL 2mol•L-1CuSO4溶液:
①反应一段时间后,有红色物质析出的是甲池中的 棒,乙池中的 棒。
②写出乙池通电时总反应的离子方程式: 。
③若乙池中通过1.2mol 电子后停止实验,则乙池中共可收集到气体的体积为(标准状况下)
2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH="-99" kJ·mol-1
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH="-99" kJ·mol-1
请回答下列问题:
(1)图中A、C分别表示_________、_________,E的大小对该反应的反应热有无影响?_________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?_________,理由是__________________;
(2)图中ΔH=_________kJ·mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒氧化物VO2;四价钒氧化物再被氧气氧化。写出该催化循环机理的化学方程式_____________________________;
(4)已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3mol SO3(g)的ΔH_______(要求计算过程)。
下表为元素周期表中的一部分.用化学式或元素符号回答下列问题:
| IA |
ⅡA |
ⅢA |
ⅣA |
VA |
ⅥA |
ⅦA |
0 |
|
| 2 |
⑥ |
⑦ |
||||||
| 3 |
① |
③ |
⑤ |
⑧ |
⑩ |
|||
| 4 |
② |
④ |
⑨ |
(1)10种元素中,化学性质最不活泼的是__________(填元素名称)。
(2)在①②⑤的最高价氧化物的水化物中,碱性最强的是__________(填化学式)。
(3)元素⑦的常见的氢化物的化学式为____,该氢化物常温下和元素②的单质反应的离子方程式是:_______________________,该氢化物与元素⑧的单质反应的离子方程式是___________________________。
(4)①和⑨的最高价氧化物对应的水化物化学式分别为___________和_______。
(5)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为__________________
(6)⑧与⑨分别与H2形成的氢化物的稳定性:__________,(用化学式表示)最高价氧化物对应的水溶液的酸性:_______________。(用化学式)
Ⅰ中国有广阔的海岸线,海水的综合利用大有可为,海水中溴含量约为65mg/L,从海水中提取Br2的工艺流程如下: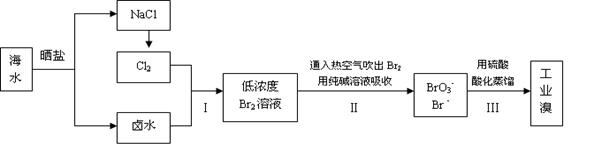
(1) 步骤Ⅱ通入热空气或水蒸气吹出Br2,利用了溴的;
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(2) 请写出步骤Ⅱ中反应的离子反应方程式;
(3) 实验室分离溴水中的溴还可以用萃取法,下列可以用作萃取剂的是;
A.乙醇 B.四氯化碳 C.烧碱溶液 D.苯
Ⅱ(1)目前世界上60%的镁单质是从海水中提取的。以下是海水中提炼金属镁的简易流程图(结合工业生产实际,在括号内填写需要加入物质的化学式,方框内填写生成物质的化学式)
(2)海带中含有碘离子,常用过氧化氢、稀硫酸和淀粉来检验其阴离子,其主要反应的离子方程式为。
按要求回答问题:
Ⅰ(1)硫酸酸化的高锰酸钾溶液与草酸反应离子方程式
(2)硫代硫酸钠与硫酸反应的化学方程式
Ⅱ工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,已知CH4、H2和CO的燃烧热(△H)分别为−890.3kJ∙mol−1、−285. 8 kJ∙mol−1和−283.0 kJ∙mol−1,则生成1m3(标准状况)CO所需热量为
kJ
Ⅲ 请写出下列物质电子式
CO2 H2O2 NH4Cl N2H4
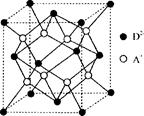
有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等子中子数。R是由A、D两元素形成的离子化合物,其中A+与D2一离子数之比为2:1。请回答下列问题:
(1)A元素形成的晶体内晶体类型应属于(填写“六方”、“面心立方”或“体心立方”)堆积,空间利用率为。
(2)C3-的电子排布式为,在CB3分子中C元素原子的原子轨道发生的是杂化,CB3分子的VSEPR模型为。
(3)C的氢化物在水中的溶解度如何,为什么具有这样的溶解性。
(4)D元素与同周期相邻元素的第一电离能由大到小的关系是:
(用元素符号表示);用一个化学方程式说明B、D两元素形成的单质的氧化性强弱:。
(5)如图所示是R形成的晶体的晶胞,该晶胞与CaF2晶胞结构相似,设晶体密度是p g·cm-3试计算R晶体中A+和D2-最短的距离。
(阿伏加德罗常数用NA表示,只写出计算式,不用计算)