化学实验兴趣小组在实验室进行氢气在氯气中的燃烧实验。
(一)设计如下图所示装置I制备和收焦干燥纯净的氯气以备后续实验;
烧瓶中发生反应的离子方程式为 ;
请根据实验目的将装置I中虚线框内装置补充完整并在括号内注明所需试剂;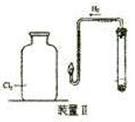
(二)在上图所示装置Ⅱ中,在试管中先加入过量铁粉,再滴入少量CaSO4溶液,最后加入一定量稀盐酸,塞上胶塞,观察到有大量气泡产生。
①检查制取氢气装置气密性的操作方法是
②当点燃氢后,将导管伸入盛有氯气的集气瓶中,观察到的现象是
(三)当氢气停止燃烧后,取出导管,同学们进行了分组探究实验。A组同学发现制氢气后的试管中还有较多固体剩余,同学们将足量氯气通入试管中,发现固体全部消失,但未观察到有气泡产生,请解释可能原因(用离子方程式表示); ;B组同学向集气瓶中注入适量水,用力振荡后,向中满入少量Na2SO3溶液,发现溶液中没有出现黄色沉淀,但再向溶液中滴入稀盐酸酸化的氯化钡溶液后,生成了白色沉淀。[已知Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O],同学们分析是由于集气瓶中还有少量氯气残留的缘故。可以解释该实验现象的两个离子方程式是:
①
四种短周期元素A、B、C、D的性质或结构信息如下:
信息①原子半径大小:A>B>C>D
信息②四种元素之间形成的某三种分子的比例模型及部分性质:
请根据上述信息回答下列问题。
(1)B元素在周期表中的位置,请写出BC2分子的电子式。
(2)A所在周期中,E元素的单质还原性最强,F元素的某些盐类常用作净水剂。E单质与甲反应有化合物X生成。请写出以下两个反应的离子方程式。
①A元素的单 质与物质甲发生的反应。
质与物质甲发生的反应。
②F、C两种元素组成的化合物Y可作为高温结构陶瓷材料,X与Y两种化合物在溶液中发生的反应。
(3)物质丁的元素组成和甲相同,丁分子具有18电子结构。向盛有一定浓度丁溶液的试管中,逐滴加入用少量稀硫酸酸化的硫酸亚铁溶液。滴加过程中的现象是 :
:
①浅绿色溶液变成深棕黄色,②有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,并放出较多热量,继续滴加溶液,静置一段时间,③试管中出现红褐色。向其中再滴入稀硫酸,红褐色变为黄色。请用化学方程式或离子方程式①、②、③中加点的字。
①② ③。
③。
某研究性学习小组的同学为在实验室再现二氧化硫催化氧化的过程,并制取少量三氧化硫晶体,设计了如图所示的装置。已知三氧化硫遇水生成硫酸并放出大量热,容易形成酸雾,工业上常用浓硫酸吸收三氧化硫。
试回答:
(1)已知6.4 g 二氧化硫被氧气氧化成气态三氧化硫,放出9.83 kJ热量。反应的热化学方程式为____________________________________________________;
(2)A装置可用来观察二氧化硫和氧气的进气量。实验时使A中氧气导管冒出的气泡与二氧化硫导管冒出的气泡速率相近,其目的是___________________________;
(3)检查完装置的气密性且加入药品后,开始进行实验。此时首先应该进行的操作是________________________________。
(4)C装置用来收集三氧化硫,若用a g铜跟足量浓硫酸反应制二氧化硫,实验结 束时得到b g 三氧化硫,该实验中二氧化硫的转化率不小于_________________;
束时得到b g 三氧化硫,该实验中二氧化硫的转化率不小于_________________;
(5)为了减轻实验对环境的污染,请你设计尾气处理装置,绘出装置图:
__________________________________________________________ 。
。
纯碱( Na2CO3)在工业生产和生活中有重要应用,其实验室制法和工业制法如下:
Na2CO3)在工业生产和生活中有重要应用,其实验室制法和工业制法如下:
【实验室制备纯碱】
(1)将饱和NaCl溶液倒入烧杯中加热,控制温度为30—35℃
(2)搅拌下分批加入研细的NH4HCO3固体,加料完毕,保温30分钟
(3)静置、过滤得NaHCO3晶体
(4)用少量蒸馏水洗涤、抽干
(5)将所得固体转入蒸发皿中灼烧得 Na2CO3固体
Na2CO3固体
问题:
①反应将温度需控制在30—35℃,通常采取的加热方法为;控制该温度的原因是;
②静置后只析出NaHCO3晶体的原因是。
【工业制备纯碱】
③沉淀池中反应的离子方程式为 ;
④循环(I)、 循环(Ⅱ)中物质的化学式分别为 。
两种制备纯碱的方法中,共同涉及的化学反应方程式为。
某有机物X的相对分子质量小于100,1mol有机物X完全燃烧生成等物质的量的CO2和H2O,同时消耗标准状况下的O2112L。
(1)该有机物X的分子式为。
a.C4H8 b.C2H4O c.C4H8O2 d.C10H20O20
(2)甲物质是X的同分异构体,分子中含羰基和羟基,物质甲能发生如下图所示的转化: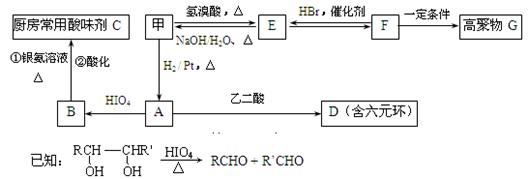 ①B的名称是。
①B的名称是。
②A→D的反应类型为,E→F的反应条件是。
③写出F→G的化学方程式:。
(3)物质乙也是X的同分异构体,1mol乙与足量的Na反应可生成1molH2,且乙不能使溴的CCl4溶液褪色,乙分子中的官能团连在相邻的碳原子上。乙的核磁共振氢谱图中有3个峰,面积比为2∶1∶1。PBS是一种新型生物降解塑料,其结构简式为 。请设计合理方案以乙为原料(无机试剂自选)合成PBS(用合成路线流程图表示,并注明反应条件)。
。请设计合理方案以乙为原料(无机试剂自选)合成PBS(用合成路线流程图表示,并注明反应条件)。
提示:①可利用本题⑵中的信息。 ②合成路线流程图示例如下: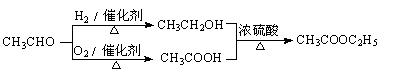
“稳定性二氧化氯溶液”是淡黄色透明液体,广泛应用于食品卫生等领域的杀菌消毒。ClO2沸点11℃,是一种黄绿色的气体,易溶于水。ClO2稳定性较差,“稳定性二氧化氯溶液”是以碳酸钠为稳定剂,有效成分为NaClO2。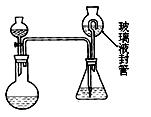
 某合作学习小组的同学拟证实其中的有效成分并测定二氧化氯的含量(用样品和酸反应产生二氧化氯的质量与样品质量的比值来衡量)。请回答下列问题:
某合作学习小组的同学拟证实其中的有效成分并测定二氧化氯的含量(用样品和酸反应产生二氧化氯的质量与样品质量的比值来衡量)。请回答下列问题: (1)为证实“稳定性二氧化氯溶液”中含有钠离子,其正确的操作步骤是:。
(1)为证实“稳定性二氧化氯溶液”中含有钠离子,其正确的操作步骤是:。 (2)为测定“稳定性二氧化氯溶液”中二氧化氯的含量,现进行以下操作:①取mg(2g左右)
(2)为测定“稳定性二氧化氯溶液”中二氧化氯的含量,现进行以下操作:①取mg(2g左右) 试样,置于烧瓶中,向分液漏斗中加入10mL盐酸溶液;②在锥形瓶中加入4g碘化钾,用100mL水溶解后,再加3mL硫酸溶液;③在玻璃液封管中加入水;④将分液漏斗中的盐酸溶液放入烧瓶中,关闭旋塞。缓慢加热烧瓶,使产生的二氧化氯气体全部通过导管在锥形瓶中被吸收;⑤将玻璃液封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用cmol/L硫代硫酸钠标准溶液滴定至蓝色消失(I2+2S2O32-=2I- +S4O62-),共用去VmL硫代硫酸钠溶液。
试样,置于烧瓶中,向分液漏斗中加入10mL盐酸溶液;②在锥形瓶中加入4g碘化钾,用100mL水溶解后,再加3mL硫酸溶液;③在玻璃液封管中加入水;④将分液漏斗中的盐酸溶液放入烧瓶中,关闭旋塞。缓慢加热烧瓶,使产生的二氧化氯气体全部通过导管在锥形瓶中被吸收;⑤将玻璃液封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用cmol/L硫代硫酸钠标准溶液滴定至蓝色消失(I2+2S2O32-=2I- +S4O62-),共用去VmL硫代硫酸钠溶液。
(Ⅰ)NaClO2与盐酸反应生成ClO2(还原产物为Cl-),该反应的化学 方程式为:
方程式为:
;ClO2通入锥形瓶与酸性碘化钾溶液反应, 二氧化氯被还原为氯离子,该反应的离子方程式为:。
二氧化氯被还原为氯离子,该反应的离子方程式为:。 (Ⅱ)装置中玻璃液封管的作用是:;如何确定烧瓶中
(Ⅱ)装置中玻璃液封管的作用是:;如何确定烧瓶中 的二氧化氯全部被锥形瓶中的液体吸收。
的二氧化氯全部被锥形瓶中的液体吸收。 (Ⅲ)“稳定性二氧化氯溶液”中,ClO2的质量分数为
(Ⅲ)“稳定性二氧化氯溶液”中,ClO2的质量分数为 (用m、c、V表示)。
(用m、c、V表示)。