纯碱( Na2CO3)在工业生产和生活中有重要应用,其实验室制法和工业制法如下:
Na2CO3)在工业生产和生活中有重要应用,其实验室制法和工业制法如下:
【实验室制备纯碱】
(1)将饱和NaCl溶液倒入烧杯中加热,控制温度为30—35℃
(2)搅拌下分批加入研细的NH4HCO3固体,加料完毕,保温30分钟
(3)静置、过滤得NaHCO3晶体
(4)用少量蒸馏水洗涤、抽干
(5)将所得固体转入蒸发皿中灼烧得 Na2CO3固体
Na2CO3固体
问题:
①反应将温度需控制在30—35℃,通常采取的加热方法为 ;控制该温度的原因是 ;
②静置后只析出NaHCO3晶体的原因是 。
【工业制备纯碱】
③沉淀池中反应的离子方程式为 ;
④循环(I)、 循环(Ⅱ)中物质的化学式分别为 。
两种制备纯碱的方法中,共同涉及的化学反应方程式为 。
如图是实验室制备SO2并验证SO2某些性质的装置图。试回答: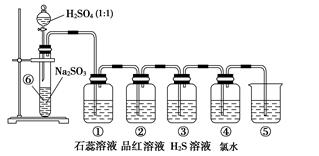
(1)⑥中发生的化学反应方程式为______________________________________
(2)⑤的作用是_______________________________________________________,
反应的离子方程式为___________________________________________________
(3)填表格(每空1分)
| 装置 |
实验现象 |
体现SO2的性质 |
| ① |
||
| ② |
||
| ③ |
||
| ④ |
某学习小组按右图在实验室制取氨气并探究铜的有关性质(部分夹持仪器未画出)。请回答: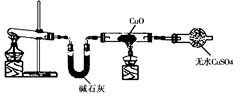
(1)制取氨气的化学方程式是。
(2)① 实验现象为:黑色CuO变为红色(生成单质a);白色无水CuSO4粉末变为蓝色; 同时生成一种无色气体,该气体无污染。请写出氨气与CuO反应的化学方程式。
②碱石灰的作用是。
(3)将上述生成的单质a在热水浴中进行4个实验,部分实验报告如下表所示。
| 序号 |
实验操作 |
实验现象 |
| Ⅰ |
稀硫酸中加入该单质a |
无明显变化 |
| Ⅱ |
硝酸钠溶液中加入该单质a |
无明显变化 |
| Ⅲ |
硫酸钠溶液中加入该单质a |
无明显变化 |
| Ⅳ |
稀硫酸中加入硝酸钠溶液 |
无明显变化 |
| 再加入该单质a |
有无色气泡;溶液变蓝 |
①实验I、II、III的目的是。
②实验Ⅳ中反应的本质是(用离子方程式表示)。
为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是可控制气体流向,用于鼓入空气的双连打气球。
(1) 实验时,先将B装置下移,使碳酸钙与稀硝酸接触产生气体,当C处产生白色沉淀时,立刻将B装置上提,使之与稀硝酸分离。该组学生设计此步操作的目的为
__________________________________。
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的化学方程式为______________________。
(3)装置E中开始时出现浅红棕色,原因是__________________________;用F向E中鼓入空气后,可观察到烧瓶E内气体颜色加深,产生上述现象的原因是__________________________________。
(4)一段时间后,C中白色沉淀溶解,其原因是_________________________________;
。(用化学方程式表示)
(5)装置D的作用是_____________________________________________________。
在进行某实验探究过程中,一些学生发现等质量的铜片分别与等体积(均过量)的浓硝酸和稀硝酸反应,所得溶液前者为绿色,后者为蓝色。
针对这种现象,学生们进行了讨论后,出现了以下两种观点:
一种认为,这可能是Cu2+浓度的差异引起的。你同意这种看法吗?(填“同意”或“不同意”),原因是。
另一种认为,呈“绿色”是Cu2+与NO2混合的结果。请你设计出一个实验方案证明之,你设计的实验方案是
已知0.3mol Cu与足量的稀硝酸反应,则被还原的HNO3的物质的量是mol。
某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。请回答下列问题:
(1)实验室制备氨气的化学方程式为;干燥氨气常用的干燥剂是。
(2)收集氨气时,请你选择氨气的进气口(填“a”或“b”)。
(3)①、若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是。
②、若装置B中的烧瓶充满干燥气体,烧杯中盛有液体,下列组合中不可能形成喷泉的是
A、HCl和H2O B、H2和H2O C、CO2和NaOH
(4)氨气在催化剂并且加热时会被空气氧化,这是工业制硝酸的第一步反应,写出该反应的化学方程式。