某课外活动小组,为研究金属的腐蚀与防护的原理,做了如下实验:将剪下的一块镀锌铁片,放入锥形瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞试液,按如图的装置进行实验,过一段时间后观察。下列现象不可能出现的是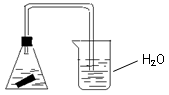
| A. B中导气管中产生气泡 |
| B. B中导气管里形成一段水柱 |
| C.金属片剪口变红 |
| D.锌被腐蚀 |
氮化硅是一种新合成的超硬、耐磨、耐高温的材料。下列对氮化硅的叙述中,正确的是()。
| A.氮化硅是分子晶体 |
| B.氮化硅是原子晶体 |
| C.氮化硅是离子晶体 |
| D.氮化硅化学式为Si4N3 |
熔化时,必须破坏非极性共价键的是()。
| A.冰 | B.金刚石 | C.铁 | D.二氧化硅 |
下列热化学方程式中,能直接表示出氯化钠晶体晶格能的是()。
| A.Na+(g)+Cl-(g)=NaCl(s) ΔH |
B.Na(s)+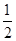 Cl2(g)=NaCl(s) ΔH1 Cl2(g)=NaCl(s) ΔH1 |
| C.Na(s)=Na(g) ΔH2 |
| D.Na(g)-e-=Na+(g) ΔH3 |
NaF、NaI、MgO晶体均为离子晶体,根据下列数据,这三种晶体的熔点高低顺序是()。
| 物质 |
①NaF |
②NaI |
③MgO |
| 离子电荷数 |
1 |
1 |
2 |
| 离子间距离/10-10 m |
2.31 |
3.18 |
2.10 |
A.①>②>③B.③>①>②
C.③>②>①D.②>①>③
某固体仅由一种元素组成,其密度为5.0 g·cm-3。用X射线研究该固体的结构时得知:在边长为10-7 cm的正方体中含有20个原子,则此元素的相对原子质量最接近于下列数据中的()。
| A.32 | B.120 | C.150 | D.180 |