(16分)乙酸丁酯(CH3COOCH2CH2CH2CH3)是具有果香味的香精,经酯化反应可进行乙酸丁酯的合成。有关物质的物理性质见下表。合成过程如下:第一步:将丁醇和过量的乙酸混合加热发生酯化反应;第二步:洗涤提纯;第三步:蒸馏提纯。
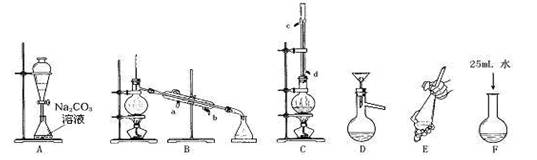
(1)上述是合成和提纯乙酸丁酯的有关装置图,请写出合成和提纯乙酸丁酯的操作顺序(填字母)C→F→ → → → 。
(2)C装置中除了装有1-丁醇和过量的乙酸外,还需要加入___________、___________。
乙酸过量的原因是__________________。装置C中冷凝管的作用是: ;
(3)步骤F:酯化反应完成后,向卸下的烧瓶中加入25mL水的作用是_____ ___ _ 。A装置中Na2CO3溶液的作用是_______ 。
(4)步骤E的操作要领是:①用一只手的手掌压住分液漏斗的塞子并握住分液漏斗;
②另一只手握住活塞部分;③ 。
(5)装置A的分液漏斗中液体分为两层,乙酸丁酯应在 (填上、下)层。
(6)第一步酯化反应过程中可能得到的有机副产物有______(写出两种物质的结构简式)。
掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
⑴写出下列仪器的名称: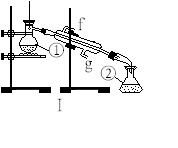
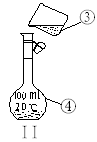
①____________;②____________;④____________;
⑵仪器①~④中,使用时必须检查是否漏水的有__________ 。(填序号)
⑶若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器有________________,将仪器补充完整后进行的实验操作的名称为;_________________ 。现需配制250 ml 0.2 mol/L NaCL溶液,装置II是某同学转移溶液的示意图,图中的错误是__________________
__________________________________________________________________(指出两处)。
欲除去硝酸钾固体中混有的少量氯化钾杂质,某学生进行如下实验操作。回答下列问题:
⑴溶解样品。该过程所需的仪器有_______________________________________________。
⑵向溶解后的溶液中加入适量的 ____________ (填化学式)溶液,使氯化钾转化为沉淀。
⑶将混合液进行过滤,过滤装置和操作如图所示,指出图中的两处错误:
① _____________________________________;
② _____________________________________。
下图装置测定中和热的实验步骤如下:
①用量筒量取50 mL 0.25 mol/L硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50 mL 0.55 mol/L NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度。
回答下列问题:
(1)写出稀硫酸和稀氢氧化钠溶液反应,表示中和热的热化学方程式(中和热数值为57.3 kJ/mol)。
(2)倒入NaOH溶液的正确操作是(从下列选出)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)使硫酸与NaOH溶液混合均匀的正确操作是(从下列选出)。
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯D.用套在温度计上的环形玻璃棒搅拌棒轻轻地搅动
(4)实验数据如下表:
①请填写下表中的空白:
| 温度 实验次数 |
起始温度t1/℃ |
终止温度t2/℃ |
温度差平均值(t2-t1)/℃ |
||
| H2SO4 |
NaOH |
平均值 |
|||
| 1 |
26.2 |
26.0 |
26.1 |
29.5 |
|
| 2 |
25.9 |
25.9 |
25.9 |
29.2 |
|
| 3 |
26.4 |
26.2 |
26.3 |
29.8 |
②近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃),则中和热ΔH=(取小数点后一位)。
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时平视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后,用另一支温度计测定H2SO4溶液的温度
四氯化硅是粗硅精炼中的中间产物,熔点-70℃,沸点57.6℃,在潮湿空气中水解生成硅酸和氯化氢。某兴趣小组在实验室里通过下图所示装置制取少量四氯化硅: 
如何检验上图气体发生装置的气密性: ______________________
A装置中发生反应的离子方程式为: ________________________
A装置中玻璃实验仪器名称为(写出两种即可):_______和_______
B中的液体为:______________F中碱石灰的作用为:① __________②________
先加热图中哪个装置:__________________原因:________________________
若实验中用12mol·L-1浓盐酸10mL与足量的MnO2反应,生成Cl2的物质的量
总是小于0.03mol,试分析可能存在的原因是:① __________② _________
(每空1分,共6分)下面是某科学兴趣小组的同学做同周期元素性质递变规律实验时,设计的一套实验方案。其中实验步骤如下:
请整理并完成实验报告:
(1)实验目的:。
(2)实验用品:
试剂:金属钠、镁条、铝条、稀盐酸、新制氯水、新制Na2S溶液、AlCl3溶液、NaOH溶液等。
仪器:、酒精灯、表面皿、试管夹、镊子、小刀、玻璃片、砂纸等。
(3)实验内容(完成下列表格中的未完成的实验现象和化学方程式):
| 实验序号 |
实验现象 |
化学方程式 |
| ① |
有气体产生,溶液变成浅红色 |
|
| ② |
生成浅黄色沉淀 |
Na2S+Cl2=2NaCl+S↓ |
| ③ |
2Na+2H2O=2NaOH+H2↑ |
|
| ④ |
剧烈反应,迅速产生无色气体 |
Mg+2HCl=MgCl2+H2↑ |
| ⑤ |
反应不十分剧烈,产生无色气体 |
2Al+6HCl=2AlCl3+3H2↑ |
| ⑥ |
开始时生成白色胶状沉淀,继而沉淀消失 |
AlCl3+3NaOH=Al(OH)3↓+3NaCl Al(OH)3+NaOH=NaAlO2+2H2O |
(4)实验结论:。
(5)请用原子结构的知识简单解释上述结论:。