几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 |
L |
M |
X |
R |
T |
| 原子半径/nm |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
| 主要化合价 |
﹢2 |
﹢3 |
﹢6、﹣2 |
﹢2 |
﹣2 |
下列叙述正确的是( )
| A.离子半径大小:r(M3﹢)>r(T2﹣) | B.R的氧化物对应的水化物可能具有两性 |
| C.X单质可在氧气中燃烧生成XO3 | D.L、X形成的简单离子核外电子数相等 |
下列有关物质分类和氧化还原的描述正确的是( )
| A.酸性氧化物一定是非金属氧化物,混合物、分散系、胶体有从属关系 |
| B.元素的单质可由氧化或还原含该元素的化合物来制得 |
| C.得电子越多的氧化剂,其氧化性就越强;含最高价元素的化合物一定具有强的氧化性 |
| D.烧碱、熟石灰均属于碱,酸、碱、盐之间发生的反应均属于复分解反应 |
下列实验不合理的是()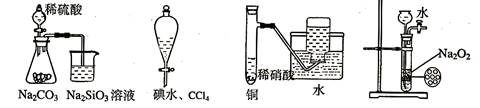
A B C D
| A.证明非金属性强弱 S>C>Si | B.四氯化碳萃取碘水中的碘 |
| C.制备并收集少量NO气体 | D.制备少量氧气 |
下列叙述正确的是()
| A.氯化铵、次氯酸钠、醋酸铵、硫酸钡都是强电解质 |
| B.电解、电泳、电离、电化学腐蚀均需在通电条件下才能进行 |
| C.红宝石、水晶、钻石的主要成分都是二氧化硅 |
| D.福尔马林、水玻璃、氨水、胆矾均为混合物 |
下列有关“化学与生活”的叙述不正确的是()
| A.烧结粘土制陶瓷涉及化学变化 |
| B.加工后具有吸水性的植物纤维可用作食品干燥剂 |
| C.点燃爆竹后,硫燃烧生成SO3 |
| D.服用阿司匹林出现水杨酸反应时,用碳酸氢钠溶液解毒 |
已知以下反应可用于去除大气中的污染:NO2+NH3 +O2—一N2+H2O(未配平)。若NO2、NH3、
O2三者恰好反应,则体积比可能是
| A.2:4:1 | B.2:1:2 | C.l:1:1 | D.l:4:3 |