门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第四周期的三种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确。根据元素周期律,下列有关X性质的描述中错误的是:
| A.X单质不易与水反应 | B.XO2可被碳或氢还原为X |
| C.XCl4的沸点比SiCl4的高 | D.XH4的稳定性比SiH4的高 |
下列有关金属的工业制法中,正确的是:
| A.制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液 |
| B.制铁:以铁矿石为原料,CO还原得铁 |
| C.制镁:用海水为原料,经一系列过程制得氧化镁固体,H2还原得镁 |
| D.制铝:从铝土矿中获得氧化铝再得到氯化铝固体,电解熔融的氯化铝得到铝 |
已知25℃时,Mg(OH)2的Ksp = 5.6×10-12,MgF2的Ksp = 7.4×10-11。下列说法正确的是:
| A.25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大 |
| B.25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者c(Mg2+)大 |
| C.25℃时,Mg(OH)2固体在同体积同浓度的氨水和NH4Cl溶液中的Ksp 比较,前者小 |
| D.25℃时,在Mg(OH)2的悬浊液中加入饱和NaF溶液后,Mg(OH)2不可能转化成MgF2 |
在一个不导热的密闭反应器中,只发生两个反应:a(g)+b(g)  2c(g)△H1<0; x(g)+3y(g)
2c(g)△H1<0; x(g)+3y(g)  2z (g)△H2>0进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是:
2z (g)△H2>0进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是:
| A.等压时,通入惰性气体,c的物质的量不变 |
| B.等压时,通入z气体,反应器中温度升高 |
| C.等容时,通入惰性气体,各反应速率不变 |
| D.等容时,通入z气体,y的物质的量浓度增大 |
下列实验现象预测正确的是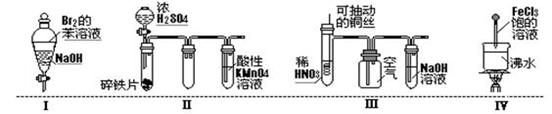
| A.实验Ⅰ:振荡后静置,溶液不再分层,且保持无色透明 |
| B.实验Ⅱ:铁片最终完全溶解,且高锰酸钾溶液变无色 |
| C.实验Ⅲ:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 |
| D.实验Ⅳ:当溶液至红褐色,停止加热,让光束通过体系时可产生丁达尔现象 |
常温下,向20 mL 0.2 mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒物质的量变化如下图(其中I代表H2A,II代表HA-,III代表A2-)。根据图示判断下列说法正确的是
| A.当y(NaOH)="20" mL时,溶液中离子浓度大小关系: c(Na+) >c(HA一)>c(H+)> c(A2- )>c(OH—) |
| B.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大 |
| C.欲使NaHA溶液呈中性,可以向其中加入酸或碱 |
| D.向NaHA溶液加入水的过程中,pH可能增大也可能减小 |